Jeg udgav for halvandet år siden, i Dec 2019, min blogserie den falske STEMI/Non-STEMI dikotmi og det forhåbentlige paradigmeskifte til OMI (occlusion myocardial infarction). Professor i akutmedicin Stephen Smith fra Dr Smith’s ECG blog og hans tidligere resident Pendell Meyers har været drivende kraft bag dette paradigme.
Hvorfor var det nu, der var behov for et paradigme skifte?
Et detaljeret svar findes på min blog. En kort sammenfatning kan jeg give herunder i punktform (kilde: Dr Smiths ECG blog OMI lecture 2020, Pendel Meyer OMI lecture 2019, og OMI manifesto 2018)
1. STEMI / NSTEMI er en falsk dikotomi: Paradigmet NSTEMI / STEMI passer dårligt med patientens outcome og en probabilistisk tankegang :
- EKG’er og (højsensitive) Troponiner kan, som alt andet, ikke fortolkes uden bedømmelse af præ-test sandsynligheden (præ TP).
- STEMI / NSTEMI er EKG-surrogatmål for det, vi egentlig gerne vil finde: OMI (dvs akut okklusion af en koronararterie der fører til irreversibel myokardieskade)
- Ved OMI er det “outcome” der er kriteriet for aktivering (Dvs høj nok post-test sandsynlighed for OMI) – ikke EKG-kriterier alene
*Bemærk: OMI / NOMI er også en “dikotomi”. En NOMI kan blive en OMI. Det er et spektrum.
Bemærk desuden: ST-elevationer er stadig høj-risiko – det er kunsten at finde OMI’er der ikke lever op til de klassiske STEMI kriterier, vi skal fokusere på
2. Vi misser for mange OMI’er i det gamle paradgime: Kort sagt, så er STEMI-kriterierne ikke sensitive nok
- Ca 40% af OMI lever ikke op til klassiske gældende STEMI-kriterier
- STEMI-kriterierne (McFarlane 2004) har sensitivitet 46% (CK-MB, lavere med troponin) og Specificitet 98%
- 25% af NSTEMI har OMI og i det nuværende paradgime har NSTEMI med OMI betydeligt højere mortalitet end STEMI- og NSTEMI uden OMI (Khan et al, 2017: Impact of total occlusion of culprit artery in acute non-ST elevation myocardial infarction: a systematic review and meta-analysis)
3. Lægen er den bedste test – ikke alene EKG’et: Ekspertise kan (og skal) læres, men vi behøver nye kriterier = OMI og probabilistisk tankegang i stedet for falsk dikotomi:
- På spørgsmålet “skal vi udføre akut PCI eller ikke?” har amerikanske PCI læger en stor variation (høj IRR) og lav specificitet (32% til 86%, snit 63%) og sensitivitet (53-83%, snit: 71%). Der er altså en stor IRR (inter-rater reliability) og i LR (ud fra gennemsnittet) modsvarer dette LR+ 1,92 og LR- 0,46 (Tran et al, 2011).
- I et andet studie spurgtes amerikanske kardiologer, akutmedicinere og PCI læger ud fra >30 EKG’er, “based on the ECG above, is there a blocked coronary artery present causing a STEMI?”. Resultatet var en IRR (kappa) på 0.33 (hvilket er ringe) . Sensitivitet og specificitet hhv for okklusion var 65% (95%CI 63-67%) og 79% (95%CI 77-81%) (interventionalisterne var bedst). Best case så modsvarer dette LR- 0,41 og LR+ 3,53 (McCabe et al 2013)
*Overstående studier er lavet uden “gestalt”-elementet (de ser ikke patienten, og tager ikke selv anamensen). Det er således en realistisk “konsult”-situation, hvor man ikke ser patienten. Du som akutlæge er nødt til at viderebringe høj kvalitetsinformation (din vurdering af præ TP) til din kardiolog / interventionalist således at så lidt “data” fra din patient tabes mellem dig og kardiologen / interventionalisten)
Hvorfor en ny blog?
Det er ikke fordi der er sket så meget på denne front. Jeg ville bare lave en lille “lommeblog” du kan finde frem, når du står med din AKS patient. Som altid råder jeg dig til at læse evidensen selv (se kilder herover), samt altid at tale med dine kardiologer og følge guidelines fra cardio.dk / dine lokale guideliens. Dette er ment som et klinisk hjælpemiddel- og en diskussions starter
Dr Smith og Dr Meyers har lavet følgende tanketræ for tilgangen til AKS. I ved, at jeg ikke er fan af algoritmer, fordi de kun fungerer på simple problemer. De er “dikotomier” og ikke spektrum. De passer med andre ord ikke ind i komplekse situationer. Når den kliniske situation er en skygge af kompleksitet, så er algoritmer med andre ord kun anvendelige, hvis du finder frem til lyskeglen, hvor de behøves og kan følges (se fx hér og hér for detaljer).
Du skal med andre ord ikke anvende denne algoritme fra start, men først i den “arm” af din differentialdiagnostik der hedder “AKS”. Med andre ord: Mis ikke de andre arme af dit differentialdiagnostiske landskab fx lungeembolien eller aortadissektionen pga denne algoritme.
Okay det er nok disclaimer om algoritmer. Lad os gå igennem og give dig de bedste links muligt til hver del af denne algoritme:
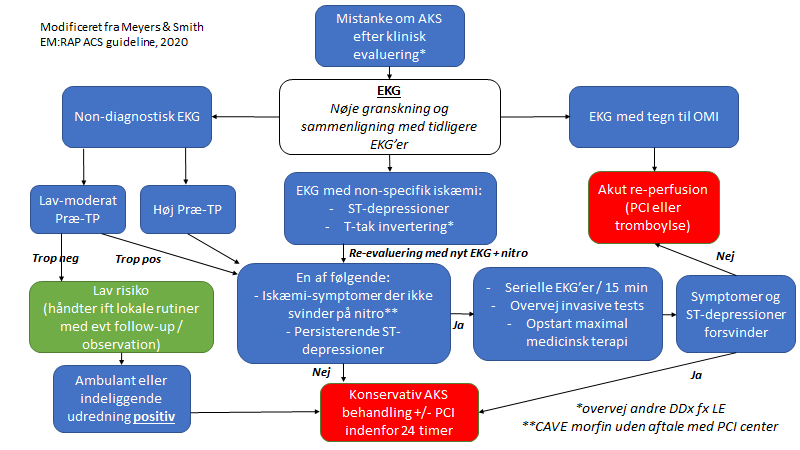
Step 1: “mistanke om AKS efter klinisk evaluering” (hvem skal inkluderes?) og AKS evalueringen med troponin og EKG
Hvordan dette helt præcist gøres er “guestimation” (estimering ud fra klinisk videnskab og gestalt). Jeg har detaljeret dette generelt i denne blog (Brick by Brick del 2) og denne blog (akutmedicineren best of del 1), og specifikt for AKS i denne blog (OMI blog del 1)
Videnskaben på dette område er særligt udforsket af Professor Rick Body fra Manchester (St emlyns), men flere andre akutmedicinere- og akutmedicinske blogs har de seneste år fokuseret på området
- First10Em (gestalt): https://first10em.com/physician-gestalt-for-acs-oliver-2019/
- Amal Mattu (kvinder): https://www.youtube.com/watch?v=FZt0ojs11Pg&t=357s
- EmCases (gestalt): https://emergencymedicinecases.com/low-risk-chest-pain-high-sensitivity-troponin/
- SGEM (ældre og troponin): https://thesgem.com/2020/01/sgem280-this-old-heart-of-mine-and-troponin-testing/ + https://onlinelibrary.wiley.com/doi/full/10.1111/acem.13933
- Rick Body: https://www.stemlynsblog.org/getting-chest-pain-evaluation-right-umecs16/ + https://www.stemlynsblog.org/risk-scores-for-cardiac-chest-pain-the-first-head-to-head-comparison/ + https://www.stemlynsblog.org/a-decade-of-diagnostics-in-emergency-care/
- David Carr og MINOCA (STEMIsh): https://drive.google.com/file/d/199HXp2EFxm9jWHyWA93QH_I7dUqZ_OT1/view
Anvender man HEART-scoren har Barbara Baccus (kvinden bag HEART-scoren) lavet en hurtig video til placering af patient i risiko-gruppe (igen: Dette er noget du først algoritmisk skal anvende, når du har bedømt at patienten er en “AKS-udredningspatient”. Den erstatter ikke klinisk bedømmelse af andre tilstande)
Ikke-brystsmerte præsentationer og atypiske præsentationer: Et problem der fortsat ikke er fuldt beskrevet, er “ikke-brystsmerte” præsentationer for AKS. Der findes hovedsageligt to grupper – hhv ældre og kvinder – hvor dette har været studeret i senere tid. Mortaliteten hos kvinder med AKS har vist sig at være højere end for mænd, og en af forklaringsmodellerne har været, at de oftere – både unge og ældre kvinder – præsenterer anderledes end vi traditionelt skulle tro AKS præsenterer som. Ældre med AKS præsenterer også oftere med “non-specific complaints” (NSC), men der foreligger meget lidt data på, hvordan vi skelner mellem troponin-slip af ikke-AKS årsag Vs AKS årsag (se SGEM artikel og podcast herover, samt kommentarerne fra Christian nickel og Rick Body). De studier der findes, viser at det formentlig ikke er fordelagtigt at tro at troponin-slip på alle ældre med NSC er AKS. Studierne har har dog været retrospektive indtil videre:
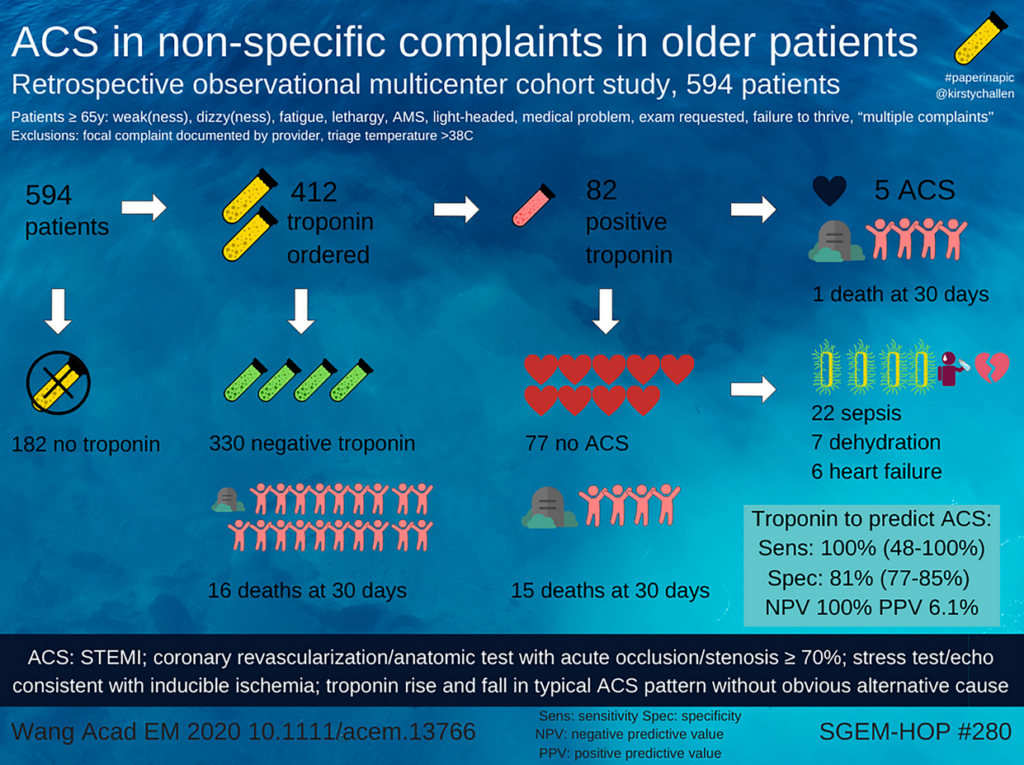
Så skal overstående algoritme (Dr Smith og Meyers’ algortime for OMI) anvendes på kvinder med non-brystsmerte præsentationer fx dyspnø- og influenza symptomer? Hvis vi skal være MERE opmærksomme på NSC hos kvinder, men IKKE skal tro så meget på troponinslip hos ældre med NSC – hvad så med ældre kvinder med NSC?
Hertil findes der endnu ingen svar. Men jeg vil mene, at algoritmen herover ikke blot skal anvendes til brystsmertepatienten, men også bør overvejes til non-brystsmerte patienten (dyspnø etc), særligt hvis det er kvinder. I evalueringen med EKG og troponin må vi dog hos ældre være villige til at lede efter andre årsager til troponinslip (da AKS ud fra den lave evidens vi lige nu har, virker til kun at være ca 1:20 troponinslip UNS), således at de ikke ligges op med “AKS” i panden på kardiologisk afdeling med en svær sepsis eller nyresvigt.
Det er probabilisme og lægekunst (sådan vil det altid være) – med bedre prospektive studier på området, kan vi i fremtiden blive endnu bedre
Hovedpointerne hér er
- Bred og åben klinisk vurdering og gestalt er altid første skridt – placer aldrig en patient i en algoritme inden du ud fra deres frit-fortalte historie og din kliniske vurdering bedømmer at deres tilstand kan være et AKS (illness script: AKS)
- Hvad vi anser som “AKS”-suspekt bør udbredes – særligt når det gælder kvinder. Kvinder præsenterer ofte poly-symptomatisk og oftere med ikke-brystsmertepræsentation – selv i ung alder præsenterer kvinder oftere end mænd med “smertefri-AKS-præsentation” (fx dyspnø, influenza-lignende symptomer etc) eller smerter på atypiske lokalisationer eller med atypisk smerte karakter
Den gamle “kvinder, diabetikere og ældre” præsenterer atypisk med AKS holder altså stadig….med en nuance:- Ældre med troponinslip, men uden stor mistanke om AKS har formentlig ikke stor risiko. Du skal, som forfatter af Geriatric Emergency Medicine bogen ,Christian Nickels med andre ord ikke tænke at “NSC” (non-specific complaints) hos ældre = AKS, bare fordi der er troponinslip (se min blog OMI del 2 om andre årsager til troponinslip). BEMÆRK: dette er retrospektiv data, og skal valideres prospektivt.
- Kvinder har oftere MINOCA (dvs AKS lignende features uden nogen okklusion), hvilket fx kan være pga SCAD (spontan coronar arterie dissektion – særligt hos yngre kvinder, se Dr Carr’s forelæsning herover) eller takutsubo
Step 2: EKG fortolkningen- og OMI
Hvilke features på EKG’et skal aktivere en samtale med PCI-centeret?
Det har jeg tidlgere samlet i denne blog (OMI del 2), og Scott Weingart / Dr Smith har samlet dette i dette ark (jf herunder), som jeg nu bærer på mig på arbejde. I OMI del 2-bloggen har jeg lagt en video, der viser de forskellige kategorier
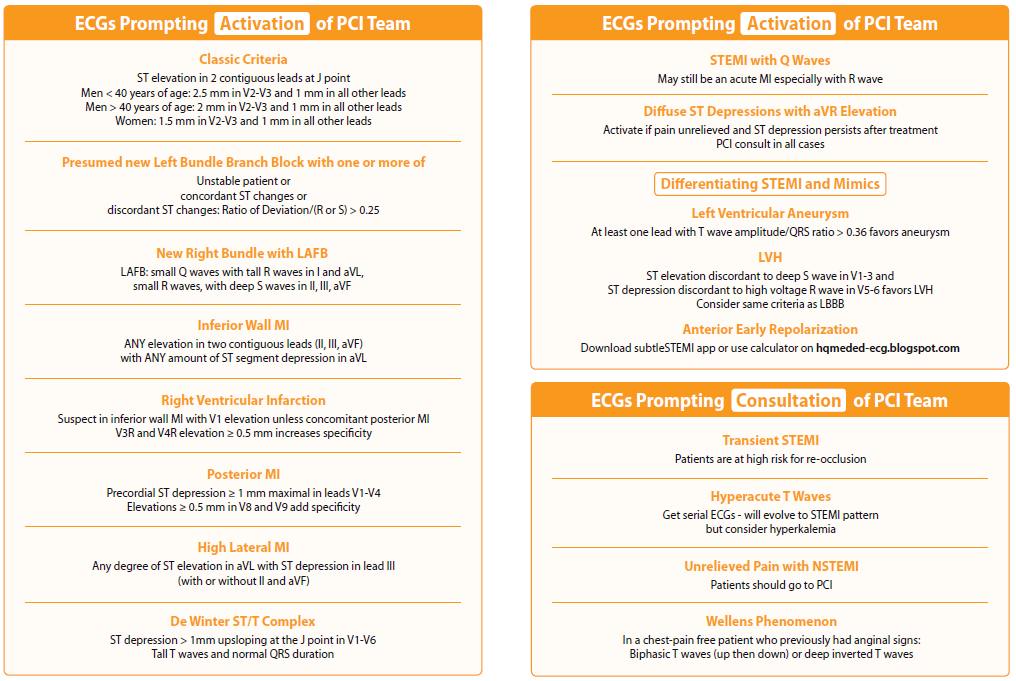
Vil du øve dig kan du fx kigge på McCabes studie quiz hér
Dr Smith beskriver, at denne quiz er et eksempel på, hvordan vi ved at øve, kan blive bedre til at spotte OMI og “lægen som test” derfor misser færre OMI’er
Hovedpointer
- STEMI-kriterierne (dvs hvor du måler mm’er i stedet for at kigge på din patient og lave en ordentlig præ-TP evaluering af deres AKS-risiko), er ikke sensitive nok for OMI. Med andre ord: Har din AKS-suspekte patient nytilkommet ST-elevation, der ikke lever op til STEMI-kriterierne, men en høj Præ-TP ud fra din evaluering – så må du gerne ringe din kardiolog / PCI læge obs OMI.
- Kend til EKG kriterier for høj risiko OMI (se Weingarts / Smiths liste herover og se forklaring i OMI manifesto’et og på min OMI blog del 2)
- Såfremt patienten ikke har uspecifikke EKG fund og/eller AKS-suspekte persisterende brystsmerter, må man re-evaluere. En normal høj-sensitiv troponin giver en lav sandsynlighed for fare, men såfremt.
- Pas på med morfin i denne gruppe, da “persisterende brystsmerter” som kriterie bliver svært-tolket (Dr Smiths lektur linket herover fra 2020, beskriver, at de har lavet studier på hans center, der viser højere mortalitet med morfin)
Step 3: Lav- og mellem risiko grupperne
Ift lav-risiko- og mellem-risiko gruppen (når man har udredt med troponin), er der de seneste år kommet en del modstand fra akutmedicinere. Tidligere har man i de fleste vestlige akutmodtagelser (muligt Danmark har været undtaget hér pga vores rimelig unikke system med “lukkede” akutmodtagelser uden fri adgang uden henvisning) udredt lav-risiko gruppen stress-test og CT af koronarkarene, samt TTE og myokardieskintigrafi.
Jeg har samlet detaljerne i disse blogs (OMI del 3, og OMI del 4)
Problemet med alle disse tests er en af mine gennemgående hoved-budskaber. Når man udfører en test på en gruppe med lav præ-TP, så er risikoen for falsk positiv ofte højere end sand positiv (se fx Justin Morgensterns blog for detaljer om dette argument). På dette argument, så er de fleste af disse tests rimeligt middelmådige, hvilket gør problemet endnu større. Slutteligt så har flere studier (COURAGE, ORBITA og det nyeste ISCHEMIA) vist at “the final common pathway” for disse sandt- og falsk positive patienter (elektiv PCI) ikke har nogen mortalitetsbenefit (symptom-benefit spørgsmålet er stadig ikke helt lukket), UDOVER den normale konservative “best medical treatment” ved CAD (coronary artery disease).
Det sluttelige spørgsmål er således hvordan vi diagnosticerer CAD – dette er (så vidt jeg ved) en risiko-bedømning, og ikke noget vi skal udføre på en akutmodtagelse. Som de siger i EmCases low-risk chest pain afsnittet: Bare fordi du ikke har AKS kan vi ikke garantere, at du har et “normalt” hjerte. Der er betydelig risiko for overdiagnostik hér, og det er derfor en shared decision making-samtale med patienten om, hvor vedkommende falder på Harm:Benefit kurven ift om de skal behandles:
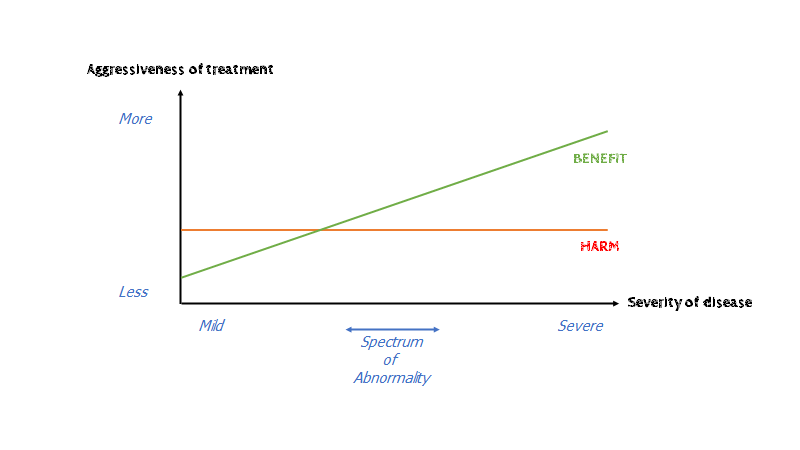
Videnskaben om test af lav-risiko patienter på akutmodtagelsen
- First10Em (Stress test): https://first10em.com/stress-test-evidence-intro/
- First10Em (CCTA): https://first10em.com/ccta-evidence/
- EmCases / First10Em (Stress test): https://emergencymedicinecases.com/cardiac-stress-testing/
- Amal Mattu (low risk patient work up): https://www.youtube.com/watch?v=FZt0ojs11Pg&t=357s + https://www.youtube.com/watch?v=j-VKs_xUA8k
- Rick Body: https://www.stemlynsblog.org/jc-are-we-fully-loded/
- Jerome Hoffman: https://www.youtube.com/watch?v=x1bfHl43lWw
Videnskab om Hs-troponiner ? Tjek Rick Bodys nye videolektur på området
Videnskaben om stenting af CAD- og det kritiserede “clogged pipe model” fx
- COURAGE
- ISCHEMIA
- ORBITA
- Dr Mandrola (om ISCHEMIA)
- Dr Mandrola (om The Clogged Pipe Model)
- Dr Mandrola (om CAD og guidelines med interessekonflikter)
Hovedbudskaber
- En “normal” AKS udredning på akutmodagelsen betyder ikke at patienten har et sundt hjerte (dvs fx CAD siger vi ingenting om)
- Er patienten efter udredning (post test sandsynlighed) bedømt som lav-risiko, skal udredningen nøje overvejes da der er stor risiko for falsk-positive og at skade din patient med stress-tests m.m
- Husk non-hjerte årsager til brystsmerter (inkl angst- og særligt iatrogent induceret angst. Læs Bernard Lowns blog og øv dig i kommunikation)
- Såfremt patienten ikke har AKS er evidensen for mortalitetsbenefit ved konservativ stenting tyndere og tyndere. Med andre ord, skal al diagnostik der leder til konservativ PCI genovervejes. Best medical treatment skal dog altid overvejes, hvis man mener at patienten har CAD – dette er ikke en akutmedicinsk opgave.
