Som man kunne læse i del 2, så er NSTEMI et bredt spektrum fra meget alvorlige med behov for akut PCI som en STEMI, og milde imod UAP-delen af spektret
- UAP / NSTEMI’er med OMI tegn (se del 2) -> omgående PCI
- UAP / NSTEMI’er uden OMI tegn -> nøjere udredning for OMI. Hvis negativ udredning, da “NOMI” eller anden årsag
Del 3 kommer til at fokusere på patienten uden sikre tegn på OMI, men som kræver nøjere udredning. Dette er majoriteten af AKS-patienterne:
fx patienten med uspecifikke EKG forandringer (fx lidt t-taks negativisering), og marginal, men signifikant troponinstigning, og en HEART-score >4-5, men under 7-10
Disse patienter behøver ofte grundig anamnese, serielle troponiner og EKG’er, og evt anvendelse af GRACE-scoren og andre tests (stress tests, myokardieskintigrafi etc) til at risikostratificere. Skulle de på noget tidspunkt få høj-risiko tegn til OMI, må man overveje udføre KAG mhp PCI. De fleste steder ligges disse patienter ind med behandling styret efter deres risikoprofil, post-test sandsynlighed og lokale guidelines (jf cardio.dk -> AKS), og i akutmodtagelsen gør vi ikke mere udredning ved dem. Risikostratificeringen vil oftest være afdelingskardiologernes opgave.
Jeg vil ikke gå længere ift håndteringen af denne gruppe – det kommer tilbage i del 4, hvor vi kigger på HEART scoren (jf evt HEART scoren del 4). Jeg vil i stedet gå lidt dybere omkring nogle af kontroverserne omkring denne gruppe mhp
- UAP
- Revaskularisering af NSTEMI
Ustabil angina pectoris (UAP)
UAP – hjertets TCI
Først et smut til neurologien. En af mine kæpheste ved akutmedicinsk bedømning af TCI (transitorisk cerebral iskæmi – også kaldet TIA: Transitory ischemic attack) er, at de kan være de sværeste diagnoser at stille korrekt uden at overbehandle – særligt hvis systemerne er lav-hieraki , fx følelsesforstyrrelser. Der findes ingen anden gold-standard for, om du har ret i din diagnose, end om patienten udvikler stroke indenfor forholdsvis kort tid efter de har set dig.
Vi har den fordel indenfor neurologisk akutmedicin, at ofte kunne erkende når det ikke er TCI ud fra anamnese, objektive fund og risikovurdering (jf fx Stone: The bare essentials: Functional symptoms in neurology., eller Suzanne O’sullivan: it’s all in your head). Dette kræver kendskab til basal neuroanatomi, og studierne på mimicks / funktionelle neurologiske lidelser (når TCI symptomer er mimicks), samt bio-psyko-social modellen (hvordan kan neurologiske symptomer opstå så hyppigt uden skade på nervesystemet)
Desuden kræver det en robust shared decision making med patienten, og egen evne til at tolerere usikkerhed.
Har man ikke alle overstående elementer, vil man i højere grad forlade sig på at behandle, hellere end at undlade. Det kræver med andre ord, betydeligt mere viden, mod / risiko tolerance, kommunikation og arbejde IKKE AT BEHANDLE, end at gøre det
Dette er almen gyldigt for de fleste tilstande i akutmedicin.
UAP (ustabil angina pectoris), er ligesom TCI’en en total klinisk risikovurdering (dog har MR-kriterierne for TCI måske ændret på dette – dette følges dog endnu ikke generelt i Danmark). Defineret ved, at der ofte ikke er nogle EKG forandringer, og at TnI ikke viser tegn til myokardie skade
Cardio.dk (tilgået nov 2019) skriver
UAP er karakteriseret ved:
- Symptomer på myokardieiskæmi opstået under hvile eller ved minimal fysisk udfoldelse.
- Crescendo angina pectoris med stigning i anfaldsfrekvens og varighed hos patienter med forud bestående kronisk, stabil angina pectoris.
UAP er en klinisk diagnose, som stilles på baggrund af anamnesen. Forbigående EKG-forandringer støtter diagnosen og har prognostisk betydning, men er ikke obligatoriske. Troponin værdier er ikke signifikant forhøjede, da tilstanden ellers klassificeres som NSTEMI.
Har UAP ændret sig efter højsensitive troponiner?
Årsagen til, at vi ved TCI (ud fra tidskriterie-definitionen) må forlade os alene på klinik og risikovurdering er fordi, der ikke (endnu) findes nogen troponin for at sige om symptomerne vi ser, repræsenterer en cerebrovaskulær okklusion (CVO).
I de seneste år, er den traditionelle troponin blevet erstattet af højsensitiv troponin. Man kan derfor stille spørgsmålet, om UAP i æraen før højsensitive troponiner, er den samme som UAP i dag? mange erfarne klinikere mener nok, at de kan genkende en UAP – men skal de / vi have opdateret deres / vores gestalt?
Studies in chest pain patients indicate that the increase in the incidence of myocardial infarction after the shift from conventional to more sensitive cTn assays is mirrored by a decrease in the incidence of unstable angina
The adoption of cTn assays with improved analytical sensitivity has resulted in an expectation that true cTn-negative unstable angina would become a rarity, if not extinct.
Our data emphasize that improved criteria to define unstable angina clearly are needed. In the context of more precise cTn assays, the current dichotomization of patients with non-ST elevation acute coronary syndrome into cTn-positive and cTn-negative entities is no longer appropriate
Eggers et al, 2018: Unstable Angina in the Era of Cardiac Troponin Assays with Improved Sensitivity—A Clinical Dilemma (Uppsala universitets sjukhus)
Overstående betyder selvfølgelig ikke, at UAP sandsynlige individer ikke skal følges op ift long-term risiko:
“These novel strategies have been fine tuned to detect MI, but not unstable angina (UA), the acute coronary syndrome (ACS) phenotype at much lower short-term risk of death and/or major arrhythmias, but at substantial long-term risk of MI. Therefore, full cardiology workup and intensive lifestyle modification and medical therapy remain crucial in UA”. Twerenbold 2017: Clinical Use of High-Sensitivity Cardiac Troponin in Patients With Suspected Myocardial Infarction
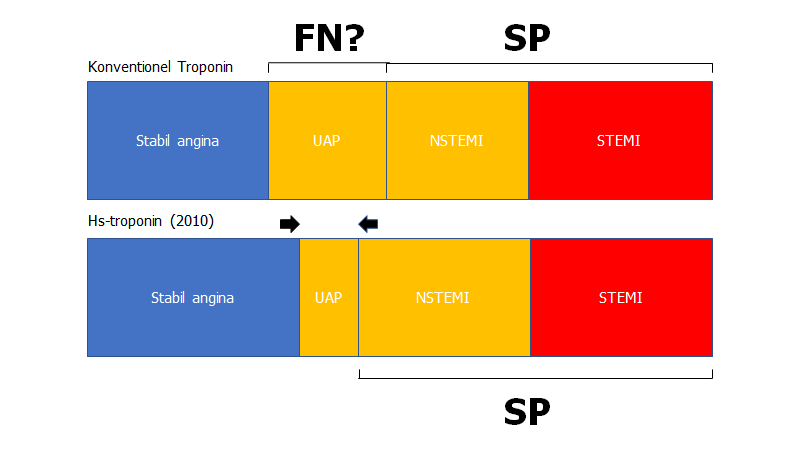
Forkortelser: FN: falsk negativ, HS: højsensitive, SP: Sand positiv, UAP: ustabil angina pectoris
Min pointe er her, at UAP nok fandtes i højere grad som følge af falsk negative troponin-serier, men at denne gruppe med de høj-sensitive troponiner og HEART-pathwayen nok er betydeligt mindre.
UAP som klinisk koncept eksisterer fortsat (crescendo angina, og patienten der hvor brystsmerterne ikke forsvinder ved stilstand efter arbejde), men spørgsmålet er, hvilken signifikans denne gruppe har i en akutmedicinsk sammenhæng (se også del 4 om “the clogged pipe analogy”), når de ikke har højsensitiv-troponin slip eller EKG forandringer.
Jeg mener endnu ikke, at vi skal slette UAP fra litteraturen, men blot, at vi altid må være skeptiske overfor gamle vaner, når ny høj kvalitets evidens kommer frem. Måske vi i stedet for Stabil angina og UAP i virkeligheden bare burde håndtere patienterne efter deres risikoprofil
Managing patients with unstable symptoms depending on their cardiovascular risk might overcome the problems related to the strict adherence to diagnostic classifications, acknowledging their inherent uncertainties. Such an approach would also take into account the fact that acute presentations of coronary artery disease encompass a continuum ranging from stable angina to large myocardial infarction with corresponding gradients of risk, rather than entities that are strictly distinct from each other.
Eggers et al, 2018: Unstable Angina in the Era of Cardiac Troponin Assays with Improved Sensitivity—A Clinical Dilemma (Uppsala universitets sjukhus)
Bottom line: Patienter skal i højere grad ses på et spektrum af kardiovaskulær risiko, snarere end i distinkte grupper. UAP diagnosen eksisterer stadig, men er blevet betydeligt begrænset i dens omfang, efter højsensitivitetstroponinens introduktion. Patienter bør behandles ud fra deres cardiovaskulære risikofaktorer.
Revaskularisering af NSTEMI i højsensitivitet-troponin æren?
I del 4 kommer jeg til at gennemgå forskellen mellem stabile og instabile plaques. Kender du ikke forskellen mellem disse to begreber, foreslår jeg, at du hopper derover først.
Vi forvirres af, at plaques kan være stabile og instabile. Det vi ser på angiogrammer (CT og KAG) hos patienten uden akutte AKS-lignende brystsmerter er oftest de stabile plaques, muligvis blandet med instabile plaques – men at skelne hér er svært, de instabile plaques lukker sjældent lumen til før de rumperer, og PCI hjælper formentligt derfor ikke disse patienter ift at forhindre AKS (og måske ikke engang symptomlindrende)
Men nu står du altså med patienten i akutmodtagelsen, med en eller anden slags brystsmerter, som du mest tror på, er AKS-relaterede og patienten har troponinslip og evt lidt uspecifikke EKG forandringer. Har de en ustabil plaque ruptur, eller symptomer sekundært til et stabilt plaque? Giver dette spørgsmål mening for patienten og vores håndtering?
(højsensitivitets) Troponiner må vel betyde myokardieskade uanset årsag?
Elevated troponin is not specific for myocardial infarction. One observational study of 615 patients with elevated troponin found that the overall positive predictive value for ACS was only 56% [18]. However, troponin is an indicator of myocardial injury independent of cause.
An elevated troponin increases the risk of short-term MACE and death regardless of cause, whether from sepsis, pulmonary embolism, chronic kidney failure or heart failure.
EmCases Ep 128: Low Risk Chest Pain
In the absence of overt myocardial ischemia, elevated cTn levels are often labeled as “false-positive” hs-cTn results, which is a misleading term. Most of these unexpected hs-cTn elevations are “true positive” for myocardial injury (rather than MI) and reflect previously undetected or underestimated cardiac disease including valvular heart disease, heart failure, hypertensive heart disease, and chronic coronary artery disease (CAD)
Twerenbold 2017: Clinical Use of High-Sensitivity Cardiac Troponin in Patients With Suspected Myocardial Infarction
Så (højsensitivt) troponinslip ift baseline betyder myokardieskade (det vigtige ord er hér “baseline” – mange kan have en højere baseline pga fx nyresvigt), uanset årsag. Det betyder, at “falsk positive”, hører til sjældenheder ifølge Twerenbold et al 2017. De noterer dog rigtigt, ved lav-risikogrupper, at “it is very important to highlight that diagnostic testing with hs-cTn should be applied to the correct population, at the optimal time and in the appropriate clinical context” (jf del 1). Det går lige i hjertet, hvis man tilhører en probabilistisk skole. Med andre ord – bestil ikke troponin på alle som en screening. Tænk altid på præ-test sandsynligheden: Although useful in patients presenting with acute chest pain, hs-cTn should not be used as a general screening test for MI in an unselected ED population.
Årsager til høje højsensitive troponiner, som ikke har med AKS at gøre er
- Høj baseline – fx
- Nyresvigt
- Hjertesvigt
- Hjerteklapsygdom
- CAD
- Non-koronar-okklusions årsager til troponinslip – fx (for fuld liste – se Twerenbold 2017)
- Takyarytmi (fx hurtig atrieflimmer)
- Myokardit
- Hjertesvigt og takutsubo
- Non-kardielle årsager fx aorta dissektion, lungeemboli, stroke, SAH, thyroidea-sygdom
- Systemiske problemer: Sepsis, rhabdomyolyse m.m
Ifølge en anden ekspert på området, Professor Rick Body, skal du dog være opmærksomme på falsk negative!: Tager din patient naturmedicin / vitaminpiller med en høj mængde biotin, er de i risiko for falsk negative (Troponin and biotin: a lethal combination? (St emlyns)) – se dette skema for at se om troponinen du anvender, er påvirket.
Okay, men de patienter vi stadig mistænker kan have en gavn af en KAG og evt PCI, som vi nu finder flere af. Hjælper revaskularisering dem?
First10Em skriver om NSTEMI / UAP ud fra hans analyse af Fanning et al, 2016:
“It isn’t clear if routine invasive management helps patients with NSTEMI and unstable angina. Invasive management clearly does not decrease the most important, objective outcome of death. There may be decreases in refractory angina and rehospitalization, but the lacking of blinding makes interpretation of such subjective outcomes tenuous. There is a small but important increase in harms such as bleeding and procedural MI using an invasive strategy”,
First10Em (https://first10em.com/revascularization-evidence/ ) konklusion fra Fanning et al, 2016 Cochrane review: Routine invasive strategies versus selective invasive strategies for unstable angina and non-ST elevation myocardial infarction in the stent era.
Revaskularisering er altså kontroversiel for denne gruppe, og ikke for alle, selvom nogle måske har gavn af det (derfor en afgørelse for specialist = kardiolog) . Justin Morgenstern konkluderer således
Outside of STEMI (or more correctly, acute occlusal MI, because not every acute coronary occlusion has ST elevation) there does not seem to be any significant benefit to invasive interventions. In NSTEMI patients, there may be a small benefit in subjective outcomes, but it is closely balanced by harms.
First10Em – Stress Tests Part 4: Revascularization and the Value of Stenting
Ligeledes skriver Steven Smith i sit OMI manifesto
Who benefits from potentially dangerous interventions designed to emergently open a coronary artery? Patients with acutely occluded coronary arteries [OMI]. There is no other theory or evidence suggesting any possible benefit from emergent reperfusion therapy other than opening an acute occlusion (or near occlusion with insufficient collateral circulation such that there is significant and irreversible acute myocardial infarction). Without the beneficial part of the intervention, patients can only receive the harms.
Patients with Occlusion MI (or near-occlusion with insufficient collateral circulation) are the only ones who benefit from emergent reperfusion therapy. And this is true no matter what their ECG shows. Those who have acute MI without occlusion (Non-Occlusion MI, or NOMI) do not need angiography emergently, although undergoing emergent reperfusion likely does not result in harm compared to urgent angiography in this subgroup. All others are exposed to the chance of harm without benefit, and do not need to be taken to the cath lab emergently
The OMI manifesto, 2018
Kan det være, at den benefit man har set i studierne på NSTEMI patienter skyldes OMI’erne (foruden den formentligt meget lille gruppe af patienter med stabile plaques der begynder at lukke helt til – demand problem)?
Så vidt mit kendskab er til litteraturen omkring KAG (hvilket er begrænset), så kan man fortsat på nuværende tidspunkt ikke sikkert skelne mellem stabile og instabile plaques. Og selv hvis vi kunne, så er de instabile plaques ikke PCI-mulige – man må behandle dem med best medical treatment ud fra risikoprofil, og PCI’e dem, hvis de skulle få plaque ruptur.
De PCI mulige plaques er altså enten
- Hyppigst: Akutte plaque-rupturer / erosioner der giver downstream akut okklusion (langt hyppigst, jf Uptodate Mechanisms of acute coronary syndromes related to atherosclerosis – tilgået nov 2019)
- Sjældent: Tillukning af lumen pga stabile plaques (CAD) uden sufficiente kollateraler
At førstnævnte har gevinst ved PCI sammen med risikomodificerende best medical treatment, er der ingen tvivl om. Om sidstnævnte har bedre effekt af PCI snarere end best medical treatment, er op til debat – selv hvis de har tropininslip. Optimalt set udfører man KAG, men udfører ikke PCI, hvis man ikke ser tegn til en af to overnævnte PCI-indikationer. I hvert fald internationalt udføres dog PCI’er oftere end det. Som jeg forstår det, så er årsagen det, at PCI-kardiologerne (som vi alle) er bundet af tradition, sandsynlighed (hvordan ved jeg sikkert, at det ikke er den læsion der giver troponin slippet?) og patientens frygt (Følgende er anbefalingsværdig læsning om dette: When evidence don’t persuade – the clogged pipe analogy).
Det virkelige spørgsmål vi egentlig vil have svar på, er dette: Hjælper høj-sensitivitets troponin patienten (POEM: patient oriented evidence that matters), eller øger vi bare antallet af falsk positive, og øger overdiagnostik?
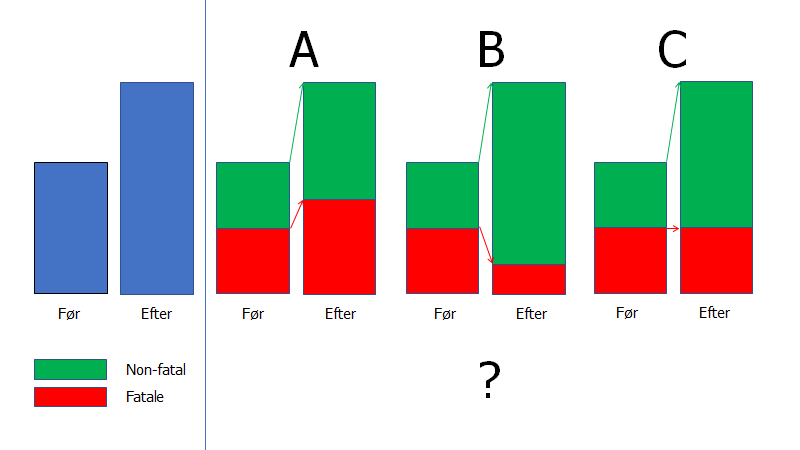
Forsimplet tegning af Overdiagnostik – grafisk fremstilt
Tænk en sygdoms incidens før og efter indførslen af en ny teknologi for diagnose (blå søjler). Måler man en stigning i antallet af diagnosticerede tilfælde med tilstanden (før Vs efter), kan dette bero på flere årsager (ud fra, den antagelse, at to ting ikke sker på samme tid):
A: Sand stigning i incidens af tilstanden: Både mortaliteten og incidencen stiger. Enten er den nye teknologi direkte farlig, eller også findes en sand stigning in incidencen af tilstanden i befolkningen
B: Effektiv test (”køber” færre døde for en stigning i non-fatale tilstande): Fald i mortalitetetn og incidencen stiger. Teknologien virker formentlig, og opfanger tilstande tids nok.
C: (ren) overdiagnostik: Uændret mortalitet, stigning i incidens
Juryen er stadig ude på den, men med en klar favorisering af, at det har gavnet med indførsel af højsensitive troponiner (anvendt i Europa siden 2010, og i USA siden 2017) med:
- Kortere ventetid på akutmodtagelsen (jf fx the HiSTORIC trial)
- Kun mild stigning i unødige revaskulariseringer
- Hjælp til at opfange patienter med signifikant CAD (coronary artery disease) som man tidligere ikke kunne finde troponinslip på (kontroversielt – jf herover)
- Diagnostik af non-AKS CAD (coronary artery disease), motiverer folk til at holde sig til sin “best medical treatment”
Vil man have detaljer om argumenterne for overstående, refereres til: Letter to the Editor – High-Sensitivity Troponin is not a Myth, and “Myth-busting” is often another Myth to be Busted (EmCrit), nov 2019
En god oversigt over højsensitivetstroponinerne og diagnostik med dem, findes i følgende studie: Twerenbold 2017: Clinical Use of High-Sensitivity Cardiac Troponin in Patients With Suspected Myocardial Infarction
Så hvilken troponin anvender I på jeres afdeling? Og kombinerer I den med en score (HEART, T-MACS, EDACS, TIMI), eller anvender I ingen score?
Hvis du ikke anvender nogen score, så kan jeg måske vække din interesse lidt med et helt nyudkommet studie fra Professor Rick Body (skaber af T-MACS scoren): Risk scores for cardiac chest pain: the first head-to-head comparison! (st emlyns) , hvor konklusionen er følgende:
This paper suggests that if you have this high sensitivity troponin I assay and you want:
- High sensitivity, highest negative predictive value and a high rule out rate – then TMACS is for you.
- Highest sensitivity and simplicity: a troponin-only strategy fits your mantra
- Highest rule-out at the cost of sensitivity; EDACS is your match, though TMACS was not so far behind
Vi begynder allerede at skrabe bunden af tilstande, hvor der er beviselig benefit ved invasive test. Men der er stadig to dele tilbage af denne blog, og en stor mængde patienter, der falder i gruppen “lav-risiko”!.
Hvad gør vi med dem? Hvordan kan vi undgå overdiagnostik på dem? Og er al fokusen på en bio-medicinsk tilgang (i stedet for at vi også tager fat i mentale og sociale delårsager) i virkeligheden i patientens bedste?
Jeg vil i del 4, og del 5 forsøge at komme problemerne nærmere og en eventuel løsning.
Bottom line: Efter introduktion af høj-sensitive troponiner, er UAP-diagnose-gruppen blevet mindre og NSTEMI-gruppen udvidet tilsvarende. Med denne udvidelse, må vi overveje, om UAP fortsat giver mening som diagnostisk gruppe, eller om den skal håndteres sammen med stabil angina som et spektrum ud fra risikofaktorer. Vi må desuden overveje, hvilke af disse lav-risiko NSTEMI’er, der skal revaskulariseres – på sygehus? ambulant? overhoved?
Højsensitive troponiner er formentlig anderledes end du hat troet, og nuancerne er værd at gå ned i studierne anbefalet i bloggen hér, for at blive bekvemme med.
Ved introduktion af OMI paradigmet, HEART-scoren og højsensitive troponiner kan man mistænke, at mængden af revaskulariseringer øger. Men spørgsmålet er, om dette kan retfærdiggøres udenfor OMI, i stedet for blot best medical treatment.

