Dato: 8/4-21 (skrevet om events seneste 3 uger siden “sportlovet”, uge 10 i Stockholm)
Dette er mit 7. indlæg på lidt mere end 1 år, om SARS-CoV-2 / COVID-19 / Corona pandemien set fra akutmodtagelsen i centrale Stockholm, Sverige. Er du ny, så er hér en ovesigt over de emner, jeg har gennemgået
- Misinformation / Disinformation, EBM, EBM 2.0 og guideliens før- under- og efter (?) pandemien:
- COVID19 second wave – hvad er anderledes denne gang? (punkt 1+2+5) (November 2020)
- Corona i Stockholm, update 14. maj 2020 (punkt 4) (maj 2020)
- Antifragility, burnout, vulnerabilitty og fejlkultur under pandemien:
- COVID19 second wave – hvad er anderledes denne gang? (punkt 3) (November 2020)
- Corona i Stockholm, update 14. maj 2020 (punkt 6+10) (Maj 2020)
- COVID19: Plan to fail and be well (punkt 1-5) (marts 2020)
- COVID-19 pandemien (marts 2020)
- Kliniske praktiske råd- og erfaringer fra vores akutmodtagelse og probabilisme klinisk bedømmelse af C19 patienten
- COVID19 second wave – hvad er anderledes denne gang? (punkt 4) (November 2020)
- Corona i Stockholm, update 14. maj 2020 (punkt 3, 5, 9) (maj 2020)
- COVID-19: Førstehåndserfaringer fra frontlinjen (marts 2020)
- Vaccination, PPE, aerosol-procedurer, epidemiologi og herd immunity
- COVID19 second wave – hvad er anderledes denne gang? (punkt 5) (November 2020)
- COVID19 kontroverser: PPE – probabilistisk fortalt, asymptomatisk spredning, sen intubation og opdaterede praktiske råd (April 2020)
- Corona i Stockholm, update 14. maj 2020 (punkt 1 + 2 + 6 + 7) (Maj 2020)
Mange af de ting, jeg har skrevet om, er almen gyldige og anvender C19-pandemien som eksempel. Således er det af værdi at læse overstående, særligt “plan to fail”-bloggen for psykisk velvære i krise og anti-fragilitet, og misinformationsbloggene ift guidelines.
Hér 1 år efter, og syv blogs senere, kan man spørge, hvad jeg dog i alverden kunne skrive om, som var relevant- eller ikke allerede er sagt bedre et andet sted?
Jeg gør det hér på min fritid (som nu er blevet mindre efter min søn kom til verdnen), og får ingen penge for det. Jeg skriver derfor kun, når jeg finder noget, jeg synes er relevant at dele for patienters- og kollegers bedste.
Mine erfaringer er ikke unikke, men som jeg forstår det på jer, mine venner og kollegaer i de danske akutmodtagelser- og sundhedsvæsen danske kollegaer, så er de anderledes (både ift mængde patienter vi ser, og ressourcer) og interessante at høre om. Derfor overvejer jeg konstant, om der er noget, der er relevant for jer at dele.
Vi kunne tale om grafen over stigningen af Corona tilfælde i Stockholm de seneste uger, og det vi kalder den 3. bølge. Jeg kunne tale om det begyndende mønstre vi ser, hvor de store ferier (og udrejse) ofte giver bølger / surge ugerne efter (denne gang “sport lovet”). Jeg kunne vise jer, at ud af de 5 sygehuse i centrale Stockholm, har 1 af dem med nød og næppe undgået katastrofe-tilstand i sidste uge, ved at flowet omdirigeres til de øvrige 3 (4) sygehuse. Jeg kunne fortælle hvordan Stockholm- og Sverige, trods mere end nok erfaring med de svære tilstande ved Corona-19 pandemien, stadig sidder i de samme problemer som de sad i, i starten af pandemien pga et dårligt designet system, der ikke taler sammen og ikke tager tilstrækkelig højde for kompleksitet. Jeg kunne fortælle, at vi lærer af vores fejl, eller i det mindste viser tegn til at vi forsøger på det, men det ville stort set være en løgn.
I stedet vil jeg denne gang invitere jer ind i mit hoved under en dag i LVT (luftvejs / corona triagen) på vores akutmodtagelse, og vise hvordan kompleksitet-, decision making, kommunikation, compassionate care og andre human factors er essentielle evner for akutmedicineren. Dette bygger på en pragmatisk tilgang, og er i højere grad en “how we do it”, og hvordan jeg resonerer, end en EBM gennemgang (dog linker jeg så vidt muligt til evidens)
I en seperat blog (kommer når jeg næste gang får tid at skrive) vil jeg forsøge at forklare, hvordan individet (front-line workeren) påvirkes i disse tider, og hvorfor Covid 19 giver os mulighed for at genskabe os selv som system, som sundhedsvæsen og som læge-kultur.
Men først – det er ikke en non-technical skill blog uden kort at nævne lidt om human factors.
Et koncept, jeg endnu ikke har fået beskrevet , men som jeg ofte anvender, og som er centralt for arbejdet i triage- og akutmodtagelsen er “fly ahead of the plane”:
Fly ahead of the plane
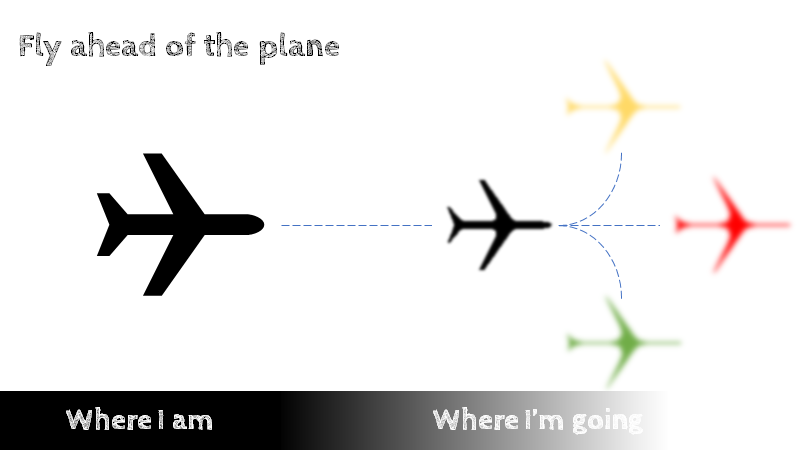
Fly ahead of the plane (fra fly-industrien, appliceret til akutmedicin) er et bredt begreb, som i essensen handler om at tænke nogle skridt frem i patientens diagnostik- og behandlingsvej, således at vejens forudseelige problemer foregribes / jævnes ud inden de opstår- eller vokser sig store. Dette kan være på individniveau- (bestille undersøgelser der allerede i triagen er nødvendige, eftersom patienten er over test tærsklen – fx bestille CT af hjernen på patienten med thunderclap headache, eller opstarte migræne behandling i triagen) og systemniveau (fx rykke mobile patienter ud i venterummet og væk fra overvågs-pladserne, så der er plads til inflowet af patienter).
Det kan foregå i stabile situationer (fx forventningsafstemning allerede i triagen med patienten, så de ved, hvad de skal vente på, og om de gider gøre det – dette sætter den næste læge i en bedre position for alliance fra start, så patienten ikke er “blevet lovet” noget som der ikke er behov for), såvel som akutte situationer (Weingart beskriver i linket herunder forskellen mellem at “kunne gøre ting” fx at have viden til at sætte et pleuradræn Vs faktisk at det bliver gjort i et real-life scenarie, hvor ting skal samles, personale skal hentes, og inden alt bliver gjort er patientens tilstand kritisk). Fly ahead of the plane ligger tæt opad visualiseringsevnen, og kan opøves som en sådan. Nogle teknikker til at opøve dette er fx
- Inden sitautionen: Visualiseringsøvelser / “arm chair flying” (se særligt Lauria, men også Bromiley og Hicks for detaljer)
- Inden situationen: “the pre-mortem”-teknikken (opfundet af gary Klein, hér forklaret af Dan Kahneman): Tænk på et scenarie, og tænk dig at alting går galt. Anvend nu 2 minutter på at skrive de ting ned om scenariet som var årsag til at det gik galt. Ændr de ting!. Dette ligger sig opad Chris Hadfields “prepare for failure”-tankegang
- Under situationen: Forcing strategi / cue til at påminde dig om at “fly ahead of the plane”
- Efter situationen: Gennemgang af scenariet både på en system 2 måde (link hér og hér og hér) og en system 1 måde (“shadow boxing” optimalt filmes scenariet, link hér og hér)
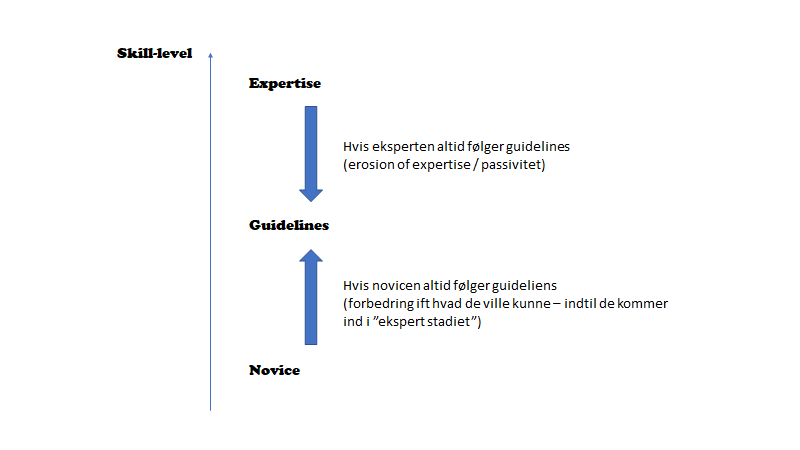
Gary Klein, en favorit hér på bloggen, og en kognitiv psykolog med ekspertise i decision making (system 1), mener at visualiseringsevnen hos eksperten formentlig er som en veludbygget heuristic / gestalt, som kommer intuitivt (hvilket ikke sker for novicen, som gennem system 2 øvelser skal øve det op).
Novicen må derfor opøve overstående bl.a. gennem scenarie gennemgang og kendskab til guidelines etc (således at system 2 bliver til system 1 tankegang gennem “deliberate practise“). Efterhånden som novicen udvikler sig, er han/hun dog nødt til at se, at selvom en guideline fortæller, at man skal følge step 1-10, så vil patienten dø inden step 6, og skal man have en chance for at redde patienten, må man hoppe direkte til step 8 og droppe step 2 som er farligt når patienten er hypotensiv. Guidelines handler om at mindske variabilitet, men nogen variabilitet er ofte godt, særligt i komplekse situationer (som vi oftest befinder os), da vi ellers er for rigide til at klare situationen optimalt.
Gary Klein forklarer
The Dreyfus model of expertise emphasizes intuition and tacit knowledge can’t be captured in procedures and rule. People might need some rules to get started in order to get started, but they have to move beyond rules in order to achieve mastery
Procedures help when you need people to reliably follow the same steps. However, that’s different from needing reliable outcomes: a blacksmith must bring the hammer down at the same point, stroke after stroke, yet we do not care if the arc of the hammer is the same each time
Gary Klein, Streetlights and Shadows
Procedures [guidelines] are most useful in well-ordered situations when they can substitute for skill, not augment it. In complex situations – in the shadows – procedures are less likely to substitute for expertise and may even stifle its development.
For en lang gennemgang af alt dette, se Scott Weingarts OODA loops and breadbaking , eller min 4 timers video om decision making, system 1- og 2, kompleksitet og kommunikation, samt lederskab og læring:
Hvor langt frem kan vi se?
Det er svært at spå, især om fremtiden
Dansk talemåde ca 1940, bl.a tilskrevet Niels Bohr
I komplekse situationer, kan vi kun se så langt, før der kommer for mange ubekendte til at have nytte af at se “frem i tiden”. I min erfaring, virker det til, at jo mere kritisk- og uforudsigelig patientens situation er, des “kortere” ind i fremtiden kan man se. På den anden side, så udvikles denne evne igennem klinisk virke, og erfarne akutlæger prøver på akutrummet ikke at følge guidelinen, men forsøger at gøre det, der skal til, for at “det guidelinen siger bliver gjort” (hvilket er logistik, og human factors m.m)
For en god artikel på hvilke strategier man kan anvende til at “fly ahead of the plane“, se fx Campbell et al, 2004, og Scott Weingarts tongue-in-cheek levering af forskellen mellem “strategy Vs logistics” og forskellen mellem “at kunne noget”, og at “få ting til at ske”, og visualisering.
Okay, det var dagens nye “human factor” bid – lad os dykke ned i min hverdag under den 3. bølge som har pågået de senste uger, og hvordan jeg håndterer den kliniske del af dette (for mine tanker angående håndtering af den psykiske- og emotionelle del se denne blog, og min nye blog om compassionate are og antifragility under Corona)
How (I) we do it (Corona 19, 3. bølge)
Igennem lidt over et år med stort set dagligt at se svært syge Corona patienter, har vi (i min gruppe som spænder fra akutmodtagelsen til intermediær afsnittene med patienter som burde være på IVA under normale forhold) opbygget en klinisk erfaring, som jeg gerne vil dele med jer. Jeg tror den letteste måde at gøre dette på, er ved at gå igennem en case og følge patientens vej igennem sygehuset
Case-beskrivelse: Kvinde i slut 40’erne, tidligere rask, kommer henvist fra en närakut (en slags walk-in klinik med almen medicinere, som ikke kender dig) pga åndenød gennem 6 dage og nu også lidt subfebrilia gennem 2 dage. Närakuten har taget en D-dimer på 1,2 og henviser obs lungeemboli. Du sidder i ydre triage og skal bestemme, hvor patienten skal hen på akutmodtagelsen
(Sidenote for helhedsbillede: der findes en “ydre ydre triage” som groft screener for alle C19 symptomer, bemandet af en sygeplejerske, som bedømmer om patienten skal til den “normale triage” eller din “C19 triage”. Du kan på klinikken “frie” dine patienter for mistanken på alle niveauer af denne triageprocess, men oftest sker det kun ved fx PCR verificeret overstået corona <6 måneder siden eller helt åbenlys anden årsag (fx svimmelhed og opkastninger i patient med nystagmus og 1 dags anamnese))
Placering af patienten: Den initielle vurdering
Når de raske er syge, og de syge er raske
Beslutningen om, hvor patienten skal placeres på akutmodtagelsen er komplex, fordi vi ikke kan placere hver patient i deres eget lille rum, isoleret fra omverdenen, indtil vi er sikre på, hvad der er galt.
Når smittetallet (R-tallet) er stigende og mængden smittede er højt i regionen, vil der være stor sandsynlighed for, at din kliniske gestalt ikke holder så godt til ”klinisk at frie for mistanke for Corona”, fordi ”alle” har Corona (hvad enten det er det, de søger for eller ej). (“frie” for Corona er hvad vi kalder det, når vi afblæser mistanken)
Med denne baggrundsviden, er der dog visse patienthistorier som er så typiske, at det er svært at tænke andet. Hér støder vi på den anden side af problemet: Anchoring, confirmation bias, premature closure, framing og diagnostic momentum. Det er svært at tvinge sig selv til at tænke andre differentialdiagnoser, når alt du ser er Corona patienter. Hér er det derfor vigtigt med forcing strategier som en bias-mitigerende strategi. Det kan fx være
- “Giv mig 3”-forcing strategien: Selvom Corona er det mest sandsynlige, tænk alligevel på 2-3 mest sandsynlige tidskritiske ikke-Corona differentialdiagnoser (du behøver ikke nødvendigvis tage parakliniske tests for dem – ofte kan man udelukke dem på klinisk mistanke). Fx ved opkastninger, sved og øvre mavesmerter, er det vigtigt også at tænke AKS, ligesåvel som kirurgiske årsager
- “Det er ikke det”-forcing strategien: En lignende strategi er at lave en slags pre-mortem på sig selv – en magisk spåkugle fra oven forklarer dig, at “den diagnose du tror det er – det er ikke det”. Dette tvinger os til at tænke på andre måder at få symptomeren til at hænge sammen (sidenote: Vi skal ikke som udgangspunkt tænke diagnoser i akutmedicin. Vi skal tænke symptomer- præsentationer og syndromer / symptom-konstellationer. Vi er ikke interesseret i at finde rigtig diagnose. Vi er interesseret i at lave den rigtigste beslutning ift tidskritiske tilstande i situationen med den viden vi har indsamlet. Om diagnosen er forkert, men patienten overlever, så har vi gjort vores job. Uanset hvad din kollega præget af hindsight bias forklarer)
- “Hvad udgør de sidste procent”-forcing strategien: En måde at komme ud af vores anchor på én diagnose, er ved at huske på, at summen af alle differentialdiagnoser er 100% (medmindre patienten har >1 årsag til sine symptomer – hichams dictum). Selv om du er MEGET sikker på, at dette er Corona, så vil du på din bedste dag måske skyde det til 70-80% sikkerhed. Hvad udgør så de sidste 20-30% differentialdiagnoser? og hvor stor en andel optager “tidskritiske” differentialdiagnoser? Er det over en testtærskel eller ej ud fra din post-test assesment? (her føler jeg, er et af områderne, hvor jeg til tider støder hovedet mod mine kollegaer i intern medicin. Når jeg kommer til dem med en patient, som jeg ikke mener i al sandsynlighed har en diagnose, men jeg vurderer, at deres risiko for en tidskritisk tilstand er for stor til at slippe dem. Der findes nogle områder, fx svimmelhed med BPPV, hvor de benigne tilstande er så pathognomiske, at sandsynligheden sænkes for alle andre tilstande når de rules in. For mere om dette lyt til Scott Weingarts samtale på intern-medicin podden Curbsiders om “devil in the gaps”, og hvorfor ældre patienter næsten altid ligger i 2-10% post-test sandsylighed )


Summa sumarum: Denne blanding af ”de syge er raske (har ikke C19), og de raske er syge (har C19)” gør dig meget ydmyg og liberal med undersøgelser, og ofte også behandlinger.
Forstå mig ret: De fleste Corona patienter har en rimelig tydelig signal:støj ratio (For en længere gennemgang af dette vigtige koncept, se Nate Silver: https://www.youtube.com/watch?v=eE4qCJBgfIk&t=875s ), og differentialdiagnoser kan man ofte finde frem til ved god anamnese og parakliniske undersøgelser . Men hvis støjniveauet stiger bare lidt, er vi ofte villige til at gøre mere, end tidligere med risiko for overdiagnostik- og overbehandling (og at øge støjniveauet endnu mere)
Risiko for patienten eller risiko for andre patienter
Beslutningen om placering bliver kun sværere når halvdelen af det semi-isolerede venterum (et rum, hvor alle har en glasvæg til højre og til venstre for sig, som en lille telefonboks uden dør) er fyldt med mange formentligt (men endnu ikke garanteret) Corona-frie patienter, som blot har corona-symptomer af en anden grund end Corona.
Dine overvejelser går derfor imellem det utilitaristiske (tør jeg frie denne patient med minimale symptomer for corona klinisk? Hvor meget skal til for at jeg er sikker nok, når personalet- og alle øvrige patienter sættes i fare ved en forkert bedømning? Og R-tallet er højt, så det er let at lave den forkerte bedømning) og det deontologiske (patienten er selv i risiko for Corona, jo længere tid jeg holder hende i Corona området). Desuden overvejelser om det selviske Vs altruistiske (jeg har haft C19, og hjælper gerne til med prøver og en grundig undersøgelse Vs jeg vil ikke undersøge patienten med mindre værdifulde undersøgelser fx stetoskopi heller ikke skabe ordentlig kontakt med dem ved berøring), og endda om lægens interessse Vs patientens interesse (se risk proximity af Simon Carley og “the fiduciary” af Jerome Hoffman)
Desuden er spørgsmålet om hvor du skal triagere patienten til. Med fyldte akutmodtagelser og når de rum, der normalt anvendes til triage, ofte er okkuperet af Corona patienter, er enhver bevægelse væk fra det semi-isolerede corona-venterum en potentiel risiko for din patient. Ofte tages triage-anamnesen derfor i et venterummet hvor alle, kan høre hvad der tales om (selvom reglerne siger vi ikke skal gøre det, så har vi ofte ryggen imod muren). Privatliv er prisen der lige nu betales. Kun hvis du er nødt til at få tøjet af patienten vælger du at flytte patienten til et andet rum (med den risiko- og forlænget process det indebærer). Alene inflows-trykket gør, at det dog ikke altid er praktisk muligt, da det tager 5 min ekstra per patient, at flytte dem (såfremt der er rum)
Hvornår kan patienten “fries” kliniskt for C19 i triagen?
Dette er millionkroner spørgsmålet, som ingen med sikkerhed kan svare på. Nogle af faktoerne der lige nu gør dette usikkert er fx
- Asymptomatisk smitte og hichams dictum (patienten søger med én ting, men har underliggende måske asymptomatisk C19). Særligt når smittetallet (R-tallet) er opadgående i en region, må man være på vagt for dette. Særligt hvis mutationer, som ikke dækkes godt af vacciner / tidligere immunitet er stigende.
- Falsk negative PCR tests / mangel på konsensus om “gold standard” for C19
- Vaccination, tidligere C19-infektion og hvornår man kan kalde folk “immune”
- Mutationer (og sub-arter af de forskellige større mutationsfamiler: engelsk, sydafrikansk og brassiliansk) med variabel beskyttelse ved de forskellige vaccine-typer
En pragmatisk (men måske ikke sand, så tag den med et gran salt, og kommenter gerne) PTP vurdering kan være følgende i vores LVT triage:
- Højest PTP / risiko: Patient som aldrig har haft C19 / aldrig vaccineret med klassiske C19 symptomer (fx hoste, feber, myalgi, hovedpine etc som præsenterer på dag 5-14 med dyspnø og behov for ilt)
- Vis PTP / risiko: som overstående UDEN C19 symptomer (fx isoleret anginøs brystsmerte)
- Lavest PTP / risiko: PCR verificeret C19 indenfor seneste 6 måneder og/eller vaccineret x2 med >2 ugers mellemrum
Som vi dog ved med PTP, så vil symptomerne og øvrige tests afgøre, hvad post-test sandsynligheden er. Har en vaccineret patient de klassiske C19 symptomer beskrevet herover, vil det give en moderat post-test sandsynlighed for C19, og en klinisk “rule out” er formentlig ikke gangbar – særligt hvis nye mutationer (som måske ikke dækkes af vaccine- eller naturlig immunitet) er stigende.
Dog må man i højere grad overveje differentialdiagnoser som LE, bakteriel pneumoni, hjertesvigt etc, end ved patienten med høj PTP (forudsat at patienten kun har én årsag til sine symptomer og fx ikke C19 og LE)
Triage plus eller Triage light?
Lige nu er situationen den på akutmodtagelsen, at når de læger, der skal se patienten er fuldt optaget, så ligger patienterne mange timer og venter. Derfor skal du pga flaskehalse gå en balancegang som triagelæge mellem “Triage light” (hurtig vurdering), Vs “triage plus” (bestil lidt mere, og tag dybere historie, så du kan gennemgå og håndtere patietnen selv i slutnigen af din dag, når blodprøver og tests er kommet tilbage, hvis de endnu ikke er blevet set).
Optimum balancen mellem disse to ekstremer kan kaldes “triage right“, hvor vi gør det rigtige ift hvad situationen kræver, og patienten behøver. Triage-punktet er et vigtigt knudepunkt i patientens vej, og præges de i forkert retning, kan det være svært at gå tilbage (diagnostic momentum og framing for den næste læge der ser patienten), selv hvis den nye læge får vigtige andre oplysninger. Derfor føler jeg altid at god kommunikation som essentiel skill, også gælder i triagen (særligt når signalet er lavt, og/eller støjen er høj), for at få bedst mulighed vej til patienten fra start. Øvrige kommunikations-tips gennenmgås snarligt:
Case fortsættelse – triageprocessen
Du får patientens vitalparametre fra din SOSU-assistent, målt på en portabel NEWS-maskine (triagesystemet på vores hospital – i Danmark oftest DEPT)
- RF 24, overfladisk
- SAT 88% på luft (går op til 97 % på 3 L)
- BT 120/80
- P 110
- Tp 37,4 i øret
Du tænker over vitalparametrene som den test de er, og med din baggrundsviden (præ-test sandsynlighed) om patienten indtil videre. Følgende overvejelser går igennem hovedet på dig:
- Ad RF, SAT og Dag 6:
- Patienten er på dag 6, og vi ved, man ofte bliver dårligst dag 7-14 (inflammatorisk fase). Har patienten allerede nu en SAT på 88% og går kun op til 97% på 3 L ilt, er patienten i høj risiko for at intensiv ilt intervention i de kommende dage, såfremt der er tale om Corona.
- Du ved, at de portable NEWS maskiner ofte undervurderer saturationen, men signalet er hér formentligt stærkt nok til at selv, hvis du satte hende på en af de bedre overvågningspladser, hvor du kan se SAT-kurven og få en SAT måling der ligger tættere opad den, du vil få på en ABG (arteriel blodgas), ville du stadig komme under de magiske 93-95% der næsten altid kræver indlæggelse. Du markerer allerede nu i journalen, at denne patient kommer til at være indlæggelseskrævende, så huset (og regionen) kan se, hvor mange pladser, de behøver finde over dagen .
Du når i triagen, inden du skal se de 6 andre patienter, der kom indenfor seneste 30 minutter, at tage en ABG på patienten, fordi der ikke er nogle overvågningspladser, ventetiden er lang i dag, og du har behov for at vide, om denne patient skal prioriteres op til NHF og hurtig indlæggelse (fx hvis pCO2 var stigende – Du kunne have væntet på en VBG, men dette ville have taget en time, og afdelingen ønsker en ABG fra akutmodtagelsen. For tiden har vi kun en håndfuld ABG’er tilbage på akutmodtagelsen, og de er “rest-noteret” (kommer ikke lige foreløbigt), hvorfor du sparer de få du har per dag til særlige / situationer, som denne). Du får svaret: pO2 med 3 L ilt på næsebrille er 9, hvilket ikke er så dårligt på ARDS skalaen . SAT 98% på ABG med 3 L ilt.
- Du bemærker desuden, at den dårlige SAT kommer takypnø med RF 24 og overfladisk vejrtrækning. Du overvejer: Er patientens SAT vedligeholdt af takypnøen (øget work of breathing), eller har patienten høj RF på grund af smerte / angst / feber / dehydratio som er urelateret til SAT’en?
Øget vejrtrækningsarbejde er altså ikke det samme som øget Work of breathing, og under C19 er vi nødt til at kende forskel for ikke at overbehandle vores patienter. I den akutte pædiatri er vi vant til at kigge efter tegn til øge vejrtrækningsarbejde, men der er ikke samme tradition for dette ved voksne. Nogle tegn til øget work-of-breathing som du kan teste bedside ifl Martin Tobin, er nogle tegn at undersøge for: kontraktioner af sternocleiden (ikke toniske, men fasiske; mærk med fingrene) og “tracheal tug” ifb vejrtrækning, svedtendens og indtrækninger – læs hér, hér, hér og hør hér Martin Tobin for nuancer. Som alle tegn (tests med ukendt LR og IRR) skal disse ses ud fra kontekst og præ-test sandsynlighed, og overstående er mig bekendt anekdotiske ift akutmedicin settingen (se Martin Tobins eget quote herunder, der er genkendende for læsere af bloggene om probabilisme og bayesian klinisk tankegang, samt gestalt)
En anden test, der måske kan hjælpe, anvender du dig af: Du ordinerer panodil 1g (smerte- og febernedsættende), og p.n morfin 2,5 mg for den ofte morfin-krævende smerte de meget inflammatoriske patienter kan behøve. Du forklarer desuden hvad der skal gøres, og at vi skal tage hånd om hende (compassionate care / angst stillende). Du ordinerer 1 L ringer via PVK. På denne behandling (på grund af eller måske tilfældigt?) ser du senere, at pulsen går ned til 95 og RF bliver 20.
For clinicians harking after simple black-and-white rules, they do not exist and are never likely to exist. The signs need to be placed in overall context.
Martin Tobin: Why Physiology Is Critical to the Practice of Medicine – A 40-year Personal Perspective
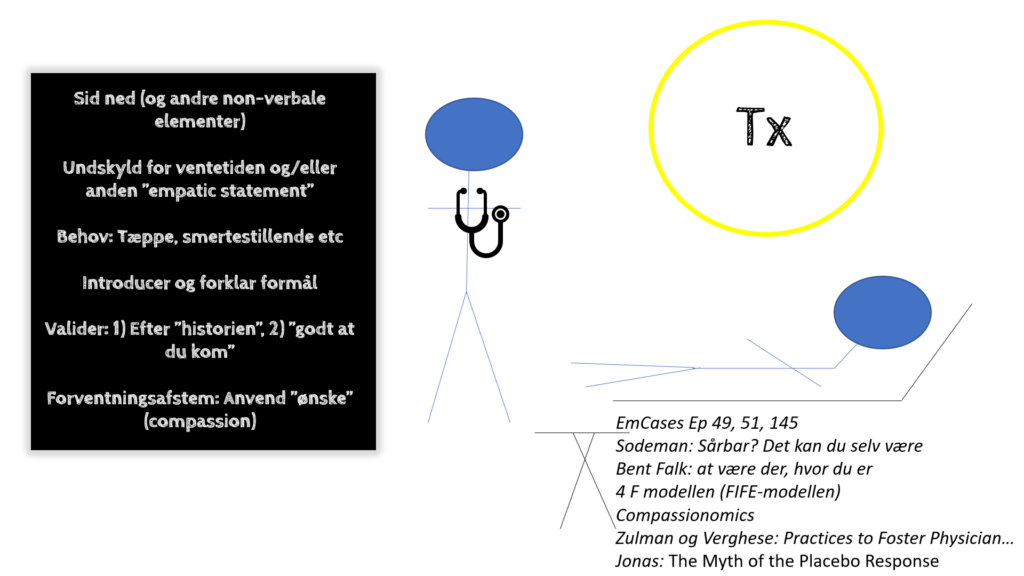
Imens du tager ABG’en taler du kort med patienten, som bekræfter historien uden at tillægge så meget mere. Du vælger ved denne patient ikke at starte med et åbent spørgsmål, men i stedet at opsummere det, der stod i henvisningen, og spørge lave en åbent slutspørgsmål: “er dette en fair beskrivelse af, hvad du søger for i dag?”. Du spørger / undersøger derefter specifikt (“lægens del”) efter følgende
- Risikofaktorer for C19 – særligt: fedme, rygning, etnicitet (formentligt ikke patofysiologisk kausalt), alder >65 år (men også komorbiditeter som tidligere DVT, immunokompromitering, hjerte- og lungesygdom m.m). Alder er formentligt den stærkeste risikofaktor for dårlig prognose / alvorlig forløb – Vi ser dog erfaringsmæssigt ikke sjældent fx unge på 30 år med BMI >25-30 eller middelaldrende rygere med risikojobs (fx taxi) have svære forløb. Covid19 (mutations-varianter?) rammer med andre ord også til tider unge på vores alder med svære indlæggelseskrævende forløb.
- Varighed af symptomer- og compassionate care: Du opsummerer henvisningen fra närakuten for patienten, og spørger om det er en rimelig udlægning af problemet i dag (patienten bekræfter). Du uddyber anamnesen og sørger for at spørge til følgende:
- Vaccinationsstatus: Vi ved stadig ikke, hvorvidt vi kan frie en patient med C19 symptomer, trods x2 vaccinationer (Sænker vaccinationen sandsynligheden for at få Corona i det hele taget? eller “bare” for at få alvorlig Corona? Og hvad med mutationerne?). Informationen er dog med til din DDx vurderingen
- Få konkret svar på varigheden af symptomer (patienten er ca dag 6-7 med C19 symptomer, ubekræftet diagnose) – de specifikke symptomer er ikke så vigtige, medmindre der er nogle der er meget atypiske (fx forvirring- eller psykose hos unge), eller støjfulde ledetråde som måske træder ud i anamnesen som atypiske ift det ”normale C19 forløb” og leder i retning af lidt bredere differentialdiagnostik (Anginøse brystsmerter, synkoper eller mavesmerter med opkastninger etc). Du ved at alle disse støjfulde ekstraoplysninger forefindes ved mange corona patienter, men nævnes de spontant ud fra en åben spørgeteknik, leder det ofte mig til en lidt bredere udredning.
- Få valideret patientens historie – du ved majoriteten af patienter du ser, sendes hjem, men at de er enormt ængstelige hjemme, hvis de er uheldige og har fået en sværere Corona med varig inflammatorisk fase. Du viser verbalt og non-verbalt bag din hjelm, siddende i hug i øjenhøjde (eller lige under), at det patienten fortæller virkelig er ubehageligt, og du forstår hvorfor de kom ind i dag (Denne lille – men evigt vigtige gestus – af compassionate care, har du flere gange overraskende set set gør at folk slipper rynken i panden, og ikke sjældent fælder tårer, og efterfølgende giver dig den største umålelige gave under Corona pandemien og i øvrigt, med et ”tak fordi du lyttede til mig”. Det påminder du dig selv om, når du har slet skjult dårlig samvittighed over, at du i dag kun tog xx patienter per time)
- Få forventningsafstemt (se fx Slade et al, og kommunikationsbloggen del 1 med appendix): Du ved at majoriteten er bange, og ønsker at vi ”fixer” eller ”gør noget” ved deres tilstand. Bedømmer du, at patienten er i lav risiko for at skulle ligges ind, forklarer du ”jeg kan se og høre, at dine symptomer er enormt ubehagelige (validering), og jeg kan godt forstå du kom ind i dag. Du er ALTID velkommen (validering). Såfremt dine symptomer er pga Corona, så vil vi helst holde dig hjemme, hvis vi ikke virkelig behøver ligge dig ind (iltbehandling, eller høj risiko for snarlig forværring). De bedste indikator for indlæggelse er dine risikofaktorer, hvor mange dage du har haft C19, og om du kan klare dig hjemme uden ilt. Under en indlæggelse, er det, som afgør hvorvidt vi behøver give dig iltbehandling, din SAT”. Du sætter herefter ofte SAT’en på fingeren af patienten og viser, hvordan iltningen er >95% både siddende og stående og ved gang, og lader selv patienten sidde med den i et stykke tid for at blive overbevist. Du afslutter med ”Jeg tror ud fra det, jeg ser her i triagen, at du ikke kommer til at blive indlagt – nogle gange bliver vi dog overrasket, når blodprøverne kommer tilbage, og vi anbefaler derfor, at du bliver her for en vurdering og mere nøje undersøgelse. Såfremt du sendes hjem, er du altid velkommen igen, og i dag 7-14 skal du have lav tærskel for at komme ind for et tjek”. Du husker desuden at nævne ventetiden, som for tiden er på 4-6 timer for den gennemsnitlige patient, alt efter hvornår på dagen, og alvorlighed af symptomerne (next step forklaring). Inden du går spørger du, om der er noget du kan gøre (empowerment af patienten til selvpleje i et usikkert- og ukendt miljø) fx bare at hente et tæppe eller slukke lyset eller give noget mad eller drikke. Din patient har ikke drukket noget hele dagen, så du henter en kold juice til hende inden du går videre til næste.
- Få indsat ”jeg ønsker” – Du nævner, at du ønsker, at du kunne tage patientens symptomer væk med en tablet eller noget andet, fordi du ser, hvor ubehageligt det er for patienten. Men at du ikke kan det. Den gode nyhed er, at det langt oftest går over af sig selv med tiden, men du ved, at det er en ringe trøst lige nu.
When taking a patient’s history, it is imperative to ask open-ended questions, enabling the patient to drive the transfer of information […] Information gleaned from leading questions runs the risk of not only being worthless, but also dangerous
Martin Tobin: Why Physiology Is Critical to the Practice of Medicine – A 40-year Personal Perspective
Skillful listening involves hearing what a patient wants to communicate, as contrasted
with getting the patient to tell you what you want to hear. Interrupting a patient’s account early in the encounter backfires.
The characteristics of the dyspnea is different: patients typically describe a sense of being unable to take a deep enough (satisfying) breath, greater difficulty in breathing in than out, a sense of oppression (suffocation) in the chest. Unlike patients with pulmonary or cardiovascular dysfunction, dyspnea in hyperventilation syndrome has a less clear-cut relationship to exercise and is less likely to improve with rest. Chest pain is frequent and sometimes mimics angina pectoris. Some patients attribute symptoms to a life-threatening disorder, such as myocardial infarction, and, fearing death, rush to the emergency room. Erroneous attribution sets off a vicious circle, causing more dyspnea and anxiety, leading to a sense of doom.
Empathetic interaction (while elucidating the history) and explanation of what is causing the symptoms is the primary therapy. Patients have a long history of alarming symptoms for which no clinician has been able to offer an explanation. Many doctors consider these patients hysterical or anxious. Patients fear their symptoms will be considered imaginary, which further contributes to their distress […] the aim is to brake the vicious cycle
Overstående teknikker har jeg gennemgået i min forelæsning fra YDAMs uddannelses dag marts 2021 (video link herunder)
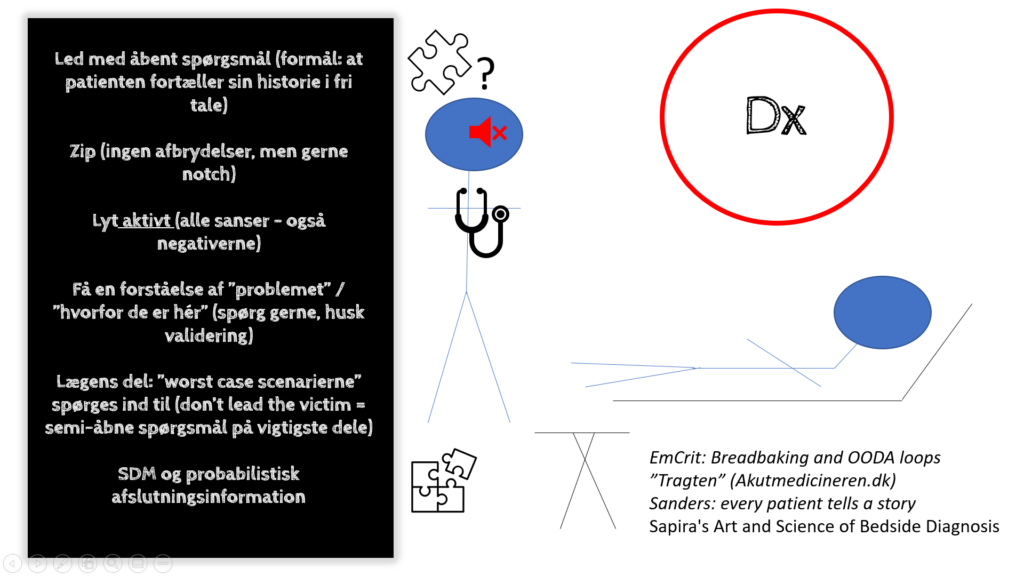
Ud fra patientens kliniske billede bestiller du følgende fra triagen
- “Pox-promenade” (at gå med saturationsmåler med patienten og se om de falder betydeligt i SAT – vær opmærksom på at holde en god saturationskurve) er ikke nødvendig, fordi patienten allerede lever op til indlæggelse i hvile
- Corona risikopanel: CRP, Leukocytter, Trombocytter, Ferritin, Prokalcitonin, Troponin, LDH, D-dimer, kreatinin, K+, Na+, Hb (særligt CRP, D-dimer og prokalcitonin er du interesseret i ift håndtering på akutmodtagelsen. Resten er interessant for forløbskontrol enten hvis patienten kommer tilbage, eller indlægges. )
- En uproportionerlig høj D-dimer ift inflammation: Er D-dimer uproportionerlig høj ift den inflammatoriske fase fx 7,2 når CRP bare er 120 (jeg ville forvente en D-dimer mellem 0-2), og har patienten en præ-test sandsynlighed der tyder på fx lungeemboli, sidder en CT skanning løst. Du venter på denne patient derfor med at bestille en CT af lungerne obs LE, men ingen konsensus findes her.
- En negativ prokalcitonin: sekundær bakteriel infektion er sjælden ved Corona. Er prokalcitoninen normal (<0,5) er sandsynligheden så lav at du aldrig opstarter antibiotika. >0,5 kræver, at den er proportionerlig med det øvrige billede
- En CRP: CRP’en der på 6. dagen er uproportionerlig høj, vil give mistanke om sekundær bakteriel infektion eller i hvert fald behov for anti-inflammatorisk behandling og måske indlæggelse trods øvrige ”ufarlige” kliniske parametre.
- Bloddyrkning: er originalt også med i panelet, men pga mangel, er det kun sepsis patienter som får taget bloddyrkning – som jeg forstår det, så har dette mere været en “flow”-årsag på afdelingen end en diagnostisk årsag til beslutningen om at have bloddyrkninger i panelet)
- Corona test: De findes lige nu 4 slags test at anvende. Den vigtigste – hurtig PCR’en med en turnaround tid på 2 timer – er en begrænset vare, og er diagnosen tydelig og patienten lav-risiko, anvendes den ikke. Er diagnosen mindre tydelig (fx når du gerne vil ”rule out” noget farligt ved at ”rule in” Corona, med risiko for at patienten dog kan have to ting – hickhams dictum), giver vil du ofte bestille hurtig PCR’en selvom patienten måske ikke behøves at ligges ind, da det potentielt kan spare dig for mere invasiv udredning. De 4 tests du har at vælge imellem er
- Hurtig PCR: turnaround tid 2 timer, Sensitivitet alt efter tidspunkt og hvor godt den er blevet taget, omkring 70%, og specificitet 90%. LR- 0,26 (så med høj PTP, udføres CT)
- Langsom PCR: Turnaround tid ca 24-48 timer, patienten går hjem og ringes op. Lignende accuracy som hurtig PCR
- Antigen testen (en point of care test): svar indenfor 15 minutter, må kun anvendes på lav PTP (præ-test sandsynlighed) patienter som screening. Praktisk anvendes den til alle patienter, der ikke går via C19-triagen, og som skal ligges ind. Hvis positiv tages PCR. Ukendt sensitivitet/ specificitet (dog ny data fra SSI tyder på at den er lav: høj risiko for både falsk negativ og falsk positive ved asymptomiatkse individer sammenlignet med PCR)
- Antistof i blodprøver: Ej anvendbar på akutmodagelsen, turnaround time dage.
- EKG: EKG’et venter du med at bestille , og lader sygeplejersken tilknyttet den kommende læge tage det, da patienten ikke er høj-risiko, og din éne triage-sygeplejerskes ressourcer bruges bedre andre steder.
Bottom line:
Hele triageprocessen har taget 2-10 minutter (alt efter signal:noise, ressourcer fra sygeplejersker , behov for mere end basal kommunikation etc), og selvom triagen kan gå hurtigere ved du, at når du selv er lægen, der modtager en dårlig triageret patient, som er blevet dårligt informeret, at det føles som om, at man blevet ”set up for failure” allerede inden. Den tid triagelægen har sparet, skal du nu bruge på at forklare patienten og (måske) genvinde deres tillid med renters rente. I sidste ende er det patientens tid der er vigtig (og de patienter ude i venteværelset), og sendes din patient hjem uden ordentlig besked- eller med en følelse af “ikke at være blevet lyttet til”, er der stor sandsynlighed for at de kommer tilbage i morgen.
Jeg har for nyligt i et lektur forklaret overstående, og hvordan jeg mener, at vi må brede vores forståelse for kommunikation som den bedste test- og terapi vi har (også i akutmedicin), for majoriteten af patienterne (obs: svensk akutmodtagelse har mange almen praksis patienter, men det bærer også over i danske forhold)
Case fortsat – blodprøvesvar og afdeling
Patienten har nu ventet i 2 timer. Der er en lang kø på akutmodtagelsen for at se en læge på en af de ca 10 læge-sygeplejerske teams (sjældent akutlæger, mest HU almen praksis-, HU intern medicinere eller KBU’ere), som hver har 2-6 patienter kørende på samme tid. Køen er lige nu 25 patienter uden team, og det er begyndt at blive aften, hvor mængden af teams reduceres til 6. Pladserne, der kom under dagen, er – som solen, der kort kigger frem bag skyerne – snart opslugt, og muligheden for at presse patienter ind, forsvinder (overnatning på akutmodtagelsen har været reglen de seneste uger for mange iltkrævende Corona patienter).
Du fik desuden at vide inden vagtstart, at et af de største hospitaler i Stockholm har gået i ambulancestop, hvorfor alle vores eventuelle pladser kommer til at overtages af patienter fra dette hospital, som fordeles mellem de forskellige hospitaler i regionen (dog udover ét af de fire andre hospitaler, som har særstilling).
Du holder løbende øje med dine triagerede patienter, hvis noget skulle stikke ud i prøverne inden de bliver set. Blodprøvesvar er kommet tilbage på din patient
- CRP 380
- Leukocytter 12
- Prokalcitonin 2,4
- Ferritin 2100
- D-dimer 1,7
- LDH 8 (modsvarer 133 i danmark)
- Hb 120 (modsvarer 7,4 i DK)
- Høj sensitiv Troponin T (Hs-TnT) 6
- PCR positiv for C19
Det er nu endnu tydeligere end før, at patienten skal indlægges, og du forsøger i tiden mellem at se patienter, at arrangere indlæggelsen for patienten. Hun er i høj risiko for at forværres indenfor kommende dage: dag 6 (dag 7-14 mest alvorlige), allerede iltkrævende, hyperinflammatorisk, middelalder.
EKG’et får du din triage-sygeplejerske til hurtigt at tage. Det er uden nytilkomne forandringer.
De fleste af prøverne er rimeligt proportionerlige ift præ-test sandsynligheden Dag 6 for C19. Dog er Prokalcitoninen på 2,4 og CRP 380 hhv lettere og meget uproportionerlige (en forventet CRP havde måske været 200, men det er ikke mere abnormt end at vi ser det et par gange per uge), og du overvejer opstart af antibiotika på baggrund af risiko for bakteriel superinfektion.
Fordi forløbet er lettere atypisk bestilles CT thorax (selvom du ved, at C19 lungerne gør det svært at anvende undersøgelsen til andet end LE udelukkelse, pneumothorax og tilstande med højt signal:støj fx abscess). Klinikerne på huset synes om (om ikke andet) at have CT’en til proportionerlighedssammenligning ift CRP’en, og det videre forløb. Det er ikke en kamp jeg tager med dem i dag.
Du har set patienter blive dårlige hurtigt (over minutter til timer med stigende iltbehov, særligt med højt work of breathing). Selvom din patients RF faldt på smertebehandling, så overvejer du stadig hvilke behandlinger, der skal indsættes på akutmodtagelsen. Protokollen er lige nu således for den indlæggelseskrævende Corona patient (IKKE dem der går hjem – dog kan denne grænse mellem indlæggelse- og udskrivelse fra akutmodtagelsen synes at bølge frem og tilbage fra dag til dag. Med andre rod, så vil den patient du opstarter i eliquis i dag, ikke skulle have det gjort i morgen. Dette er formentligt ikke noget problem i dine øjne, da NNT : NNH kurven ikke er mest favorabel for “grænselands”-patienterne og nedefter, men snarere høj risiko patienterne, som din patient)
Iltbehandling
Der findes forskellige slags iltbehandling, alt efter patientens behov. Du gennemgår i hovedet disse, som du efterhånden er blevet bekendt med over det seneste år
Kriterierne for at gå op et skridt er arbitrært (ud fra fysiologisk- og rationel bedømning) sat ved
- 1: RF >30 trods smertestillende- og febernedsættende
- 2: 7 L ilt for at holde målsaturation (moderat-svær KOL: 88-92%, alle andre >94%)
- 3: Hurtig forværring / iltkrav (”delta-kriteriet”)
- 4: Udtrætning / Retention (pCO2 stigning)
- 5: Komorbiditet (fx hjertesvigt eller KOL) der kræver fx BiPAP eller CPAP
Formålet med iltbehandlingen at forhindre den farlige hypoxi (bemærk, at hypoxi er nedsat iltning af væv, hvorimod hypoxæmi, er nedsat iltning i blodet. Relationen mellem de to størrelser, er diskuteret i Martin Tobins artikel EmCrit podcast)
Dette gøres primært ved tilførelse af luft med høj FiO2 (dvs flow er mindre vigtigt, hvis det ikke afstedkommer en FiO2 stigning) for at forhindre hypoxi (se dansk lungemedicinsk selskab for detaljer om normal iltbehandling, og se også gerne deres Corona guide som aktuelt er i version 5)
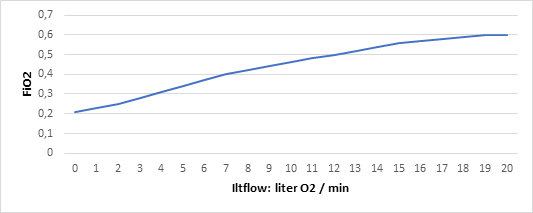
Er patienten dog i enten svært type 1 lungesvigt (hypoxisk svigt) eller type 2 lungesvigt (hyperkapnisk svigt), behøves en af følgende til at afhjælpe problemet
Jeg har hér anvist metoderne kronologisk ift hvordan vi bruger dem: Ilt -> NHF -> CPAP -> NIV -> Intubation
Hvilket skridt man starter på, afhænger af stabilitet, risiko for forværring, udtrætning, og graden- og typen af svigt. En 50 årig tidligere rask patient dag 9 med hyperinflammation og 15 L ilt for at holde SAT >90%, vil gå direkte i NIV (alternativt intubation). Derimod vil samme patient med langsom forværring til 8 L ilt, gå i NHF og starte på 15 L flow og trappe op i ilt på dette niveau indtil målsaturationen er opnået. En mellem-variant med hurtig forværring af samme patient, vil være at opstarte NHF på højere niveau fx 30 eller 45 L flow med 100% iltning, og enten trappe op i flow med 5L øgninger hvis ingen effekt, eller trappe ned i ilt, hvis der var effekt. Samme patient , men med KOL- eller begyndende pCO2 ophobning af anden årsag, vil gå i NIV direkte. Samme patient med hjertesvigt vil starte i NIV, men oftest trappes ned ganske hurtigt efter stabilisering.
Step-vis iltbehandling ved Corona 19 patienten
OBS: bemærk, at i Danmark gælder Dansk Lungemedicinsk selskabs guideline for HFNO og Corona (og lokale guidelines). Bl.a anbefales <60% ilt-mætning for ikke at skabe lungeskade. Dette fraviger vi ofte i Sverige. Desuden anvendes ROX-score til vurdering af HFNO patienten. Vi udregner mig bekendt ikke ROX-scoren, men vi kigger klinisk på work-of-breathing og risiko for udtrætning jævnført med iltning.
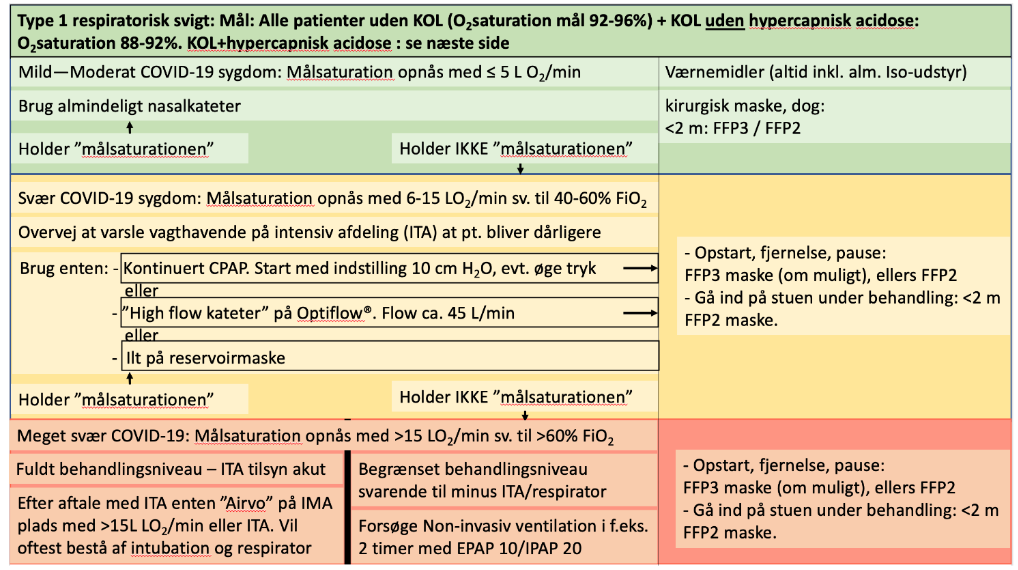
Bemærk desuden at “grænserne” for hvad der er “step up”-indikation i den virkelige kliniske hverdag afhænger af kapacitet / ressourcer. Har du ingen pladser til intubation eller NIV, så kører du fx iltningen op >60%, og forsøger at holde patienten indenfor parametrene (uvist om dette er POO: Patient orientet outcome eller MOO: Monitor oriented outcome, da studier ikke findes på området – dette er den fortsatte usikkerhed ved Corona19, og det vil ikke overraske mig, at “det fysiologiske argument” ikke holder, når studier udkommer på området, og at vi måske skader patienter på denne måde mere end hvis vi lod dem være hypoxiske, men ikke hypoxæmiske). “Grænserne” gælder dermed i ideal-situationer, hvilket vi er langt fra i Stockholm lige nu
Tag derfor nedenforstående som inspiration, men følg den danske anbefaling (selvom det meste er i overenstemmelse med danske forhold):
- Skridt 1: Iltbehandling
- Typer af behandling: Iltbehandling på næsebrille (0-4L), venturi-maske (3-6L), oxymaske (0-10L) eller non-rebreather (10-15 L) alt efter FiO2 behov.
- Observandum: Ligger patienten længe med iltbrille vær da opmærksom på tryksår, og udtørring af slimhinder (kold luft uden fugtning)
- Optrapning til næste niveau (se kriterier herover)
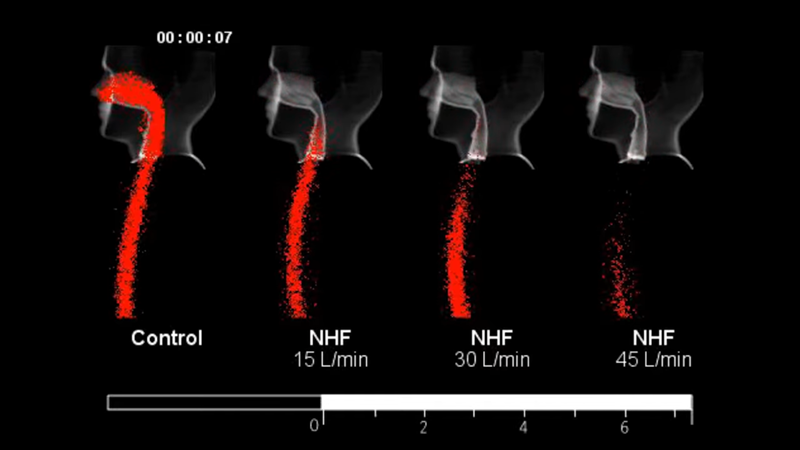
- Skridt 2a: High flow nasal oxygen (HFNO) – hos os kaldet NHF (Nasal high flow oxygen) – (hvis retention af pCO2 hoppes dette skridt over, og man går direkte til NIV eller intubation, https://www.youtube.com/watch?v=oVv36IZZf7U )
- Fordele ift normal iltbehandling: NHF har de fordele, at
- 1) den er mere behagelig (larmer mere, men har fugtet- og opvarmet luft / ilt, hvilket gør, at folk kan holde længere på den)
- 2) Fjerner ”deadspace”: når du ånder ind / ud, er de første dele af dit åndedræt brugt på at bevæge luft igennem deadspace (anatomi, hvor der ikke findes mulighed for iltoptag: mund, pharynx og trachea). NHF giver et flow-tryk (mellem 0-60 L/min), som i teorien fjerner mere og mere dead-space som man går op i tryk, således at åndedrættet du trækker ind anvendes til iltning, i stedet for dead-space transport.
- 3) Muligvis giver lidt PEEP / EPAP på 0-6 mmH2O (trykket når udover dead-space hele vejen ud i lungerne og sørger for et konstant tryk)
- Anvendelse: Jeg nævner det med dead-space herover – ikke fordi det nødvendigvis er helt evidensbaseret (det er hypotesen bag udstyret, men et rationalistisk / fysiologisk argument fra et device firma er ikke noget jeg køber med det samme (https://www.thesgem.com/2018/04/sgem-xtra-the-danger-within-us/ )) – men fordi det er en god analogi til hvordan du skal anvende apparatet. Det giver nemlig logisk mening nu, at du skal fjerne deadspace først, og siden øge iltningen. Det vil sige (variation kan forefindes i metoden at anvende NHF på – dette er min metode- og mange af mine kollegaers metode)
- Step 0: set-up af NHF (gøres af sygeplejerske – husk varmen- og fugten på ilten, for at det ikke er uudholdeligt)
- Step 1a: Øg tryk fx med 15 L/min ad gangen indtil 45 L. Herefter øges 5 L / min, da færre tolererer trykket >45-60 L/min (Alt efter tilstand trapper man op hurtigere fra 15-45 L/min og justerer ilten derefter)
- Step 1b: Øg ilt til målsaturation er opnået (alt efter hvor dårlig patietnen er, starter man gerne på 100% og trapper ned, snarere end at gå nedefra og op).
- Step 2: når patienten har stabiliseret sin SAT, kan man altid finjustere tryk- og iltindstillinger (ud fra princippet herover, bare omvendt, når man justerer ned: ilt ned -> tryk ned)
- Step 3: Monitorer SAT, RF og eventuelt pCO2 på ABG/VBG og indstillingerne accepteres af patietnen (dette er en af anledningerne til at man ikke bare fjerner alt dead-space fra start ved alle, ved at køre 65 L/ min)
- Step 4: Hvis patienten lever op til en af de kriterier sat herover (RF >30, SAT under målsaturation trods indstillingerne i step 1 og 2, hurtig forværring) vil man gå igennem step 1-3 igen med nye indstillinger (fx nu øget fra 15 -> 30 L flow, og trap ilten op til målsaturationen).
- Step 5: Stiger patienten i pCO2 ELLER er patienten ”maxet ud” i NHF indstillinger (ofte 65 L med høj iltmætning fx 70-100%), og kan alligevel ikke holde sin iltning til målsaturationen, må man gå til næste skridt (enten NIV, CPAP eller Intubation)
- Set up: For setup se youtube video demonstrationer (dette er som regel din sygeplejerske der styrer dette)
- Fordele ift normal iltbehandling: NHF har de fordele, at
- Skridt 2b: CPAP og ”götterfunken”: CPAP apparater giver et PEEP / EPAP som primært fungerer ved hypoxisk ARDS uden pCO2 retention (husk ”rule of two’s” https://www.youtube.com/watch?v=t9GfGCckx-Y – EPAP / PEEP hjælper på hypoxi og anvendes fx til lungeødem Vs IPAP og deltaet mellem IPAP og EPAP hjælper med pCO2). På mit hospital løb vi tør for NHF og CPAP allerede sidste år, hvorfor vores fysiologer har McGyveret OSAS-apparater til det de kalder ”götterfunken”, som fungerer nogenlunde som en CPAP.
- Anvendelse: CPAP’en kan eventuelt anvendes hvis patienten primært har et hypoxisk problem eller har komponent af fx hjertesvigt, lungeødem eller atelektaser og har behov for lidt EPAP
- Skridt 3: NIV (NIV foregår på akutmodtagelsen, “normale” afdelinger med lungemedicinsk ekspertise, og intermediær afdelinger – modsat i Danmark, hvor det oftest er på IVA)
- Fordele ved NIV’en: Fordelene ved NIV’en er at den kan hjælpe med pCO2 retention og udtrætning. Ulemperne er, at det er ubehageligt for patienten, større risiko for tryksår og kommunikation begrænses. Ofte NIV’es patienten samtidig med proning eller lignende positionering.
- For info om hvordan den virker anbefales dette link om ”rule of two’s”: https://www.youtube.com/watch?v=t9GfGCckx-Y
- Obs: Inden NIV skal man altid overveje pneumothorax (som kan blive til en trykpneumothorax, hvis den misses). Covid-lungerne kan over tid skabe små huller og give mindre pneumothorax tilstande (er vores erfaring). Jo mere inflammatorisk, des større behov for at lave en CT eller POCUS inden eller lige efter NIV opstart (alt efter hvad klinisk tilstand tillader).
- Skridt 4: Intubation:
Uptodate beskriver følgende indikation for intubation under Covid19:
1: Hurtig progress over timer
2: Manglende bedring trods NHF >50 l flow / min og >0,6 FiO2
3: Tegn på udtrætning (pCO2 stigning, forvirring, øget work-of-breathing etc)
4: Multiorgan svigt- eller hæmodynamisk instabilitet
intubation kræver IVA afdelingspladser. Efterhånden som IVA pladserne forsvinder, bliver selekteringen af patienter, der kan havne der strammere og strammere. Dette har forårsaget en rippel-effekt på sygehusene, hvor dårligere og dårligere patienter accepteres på lavere og lavere afdelingsniveau (indtil de ender med at overnatte på akutmodtagelsen, fordi vi har bedre monitoreringsmulighed end en overbelagt afdeling med halv personalebesætning, som iøvrigt arbejder længere tid end de plejer).
Overstående kriterier gælder, men som beskrevet, er kriterie 2 noget vi oftest ikke intuberer på, og kriterie 3 vil udløse NIV først. Kriterie 4 er sjældent ved C19 i dag 7-14 og primært ved de senere forløb og/eller komplikationer (sepsis, LE, arytmi, hjertesvigt etc) til C19
Det er dog ikke alene ressource-problemer, der forklarer hele sandheden om de stramme kriterier: Vi ser desværre tidligere raske (eller med få risikofaktorer som BMI >25-30) patienter >50-60 års alderen, der efter den inflammatoriske fase simpelthen ikke kommer sig (selvom det særligt ses ved >75-80 årige). Billedet virker ikke fremmede for vores intensiv-læger. Patienten C19 dag 20-30 kan ikke komme af respiratoren (eller NIV alt efter afdelingsniveau). Om det er den tabte muskelmasse, lungerne som er ødelagte af infektionen (reversibilitets komponenten er for mig ukendt hér) eller kombinationen skal jeg ikke gøre mig klog på. Men selv når blodprøvebilledet begynder at normalisere, er den kliniske tilstand ikke i bedring. Og ofte går det sådan, at blodprøvebilledet begynder at stige igen pga nosokomiel infektion eller andre komplikationer til at ligge i respirator og på IVA. Og med de førnævnte sparsomme pladser, hvor længe tør man satse – når køen af yngre patienter med større chance er højere? Vores intensivister har det ikke let
Proning og positionering: Proning og positionering, til trods for metodens sparsomme evidens under C19 ARDS, virker det klinisk til at være en værdifuld detalje for visse patienter som tolererer det.
Sedering: CPAP, NIV og proning er ubehageligt for patienten. Når særligt de ældre patienter “maxes” ud i indstillingerne på apparaterne og intubation ikke er en mulighed (læs intubationsdelen herover), vil de ofte have behov for sedering på ikke-intensiv afdelinger. Denne sedering foregår oftest med Dexmedetomidine.
Munden: Ved NHF er det optimalt at patientens mund lukkes. Ved små børn kunne man give dem en sut i munden når de behandledes med “grise-tryne”, men vi er ikke kommet dertil, hvor vi giver sut til patienterne. Dog anbefales de at holde munden lukket når de ikke taler / spiser.
“udmaxning” og end of life: En typisk “udmaxet” oftest ældre (>65 år) patient, er patienten som ikke kan komme til ITA pga komorbiditeter / alder / pladsmangel / dårlig prognose, som får NIV med høje EPAP (til tider >20 cmH20 evt med IPAP delta alt efter retention), på dag >20, som er sederet med dexmedetomidine i proning, og kun lige holder sin SAT >90, med begyndende tegn til svigtende organsystemer. Hér træffes beslutningen ofte end of life, men følelsen af “bare en dag til, så vender det” kan hænge ved mange af mine kollegaer- og mig selv de få gange jeg har været i situationen på en afdeling. Med pladsmangel er det en balance, hvor mange dage vi ønsker at give patienten , og samtidigt velvidende, at chancen for overlevelse til lignende selvstændige livsomstændigheder formentlig er lav (lad os skyde <5%). Jeg har forsket i HLR- og neuroprognosticering, og er bekendt med problemet med “self-fulfilling prophecy”, særligt tidligt i forløbet (at uden randmomiserede studier, så giver jeg mig selv ret, når jeg siger, at patienten ikke kommer til at overleve, og jeg slukker for maskinen). På den anden side, så er lidelsen mærkbar på mange familier- og patienter, og når patienten er “maxet ud” så er det sjældent, at situationen vender uanset hvad vi gør. Og selv hvis den gør, rammes de desværre ofte af komplikationer. Palliation for patienten og løbende psykisk sparing med sundhedspersonale er essentielt alle dage, og særligt nu. For palliative tips, se fx “lille smärtis” eller geriatrisk akutmedicin bloggen, samt “mastering communication with seriously ill patients“. For håndtering af det psykiske, se del 2 af denne blogserie (om antifragilitet)
Case fortsat: Din patient kræver lige nu ilt, men er i høj risiko for forværring (dag 6, hyperinflammatorisk). Du forsøger at ligge patienten på en Corona afdeling, hvor muligheden for NHF findes, da dette er næste skridt. Der er ingen tegn til pCO2 retention og ingen akut forværring lige nu, hvorfor højere skridt ikke behøves.
Antitrombotisk behandling
Viden om antitrombotisk behandling bølger frem og tilbage. Vi anvender følgende på mit hospital for indlæggelsespatienter med C19
- D-dimer <3: profylakse dosis LMWH (4500 IE x1)
- D-dimer >3: dobbelt profylakse dosis LMWH (ofte 9000 IE x1) – ej anbefalet fra DSTH
- Verificeret LE: Fulddosis LMWH (fx 175 IE/kg tinzaparin)
Dog begynder der er komme studier på farligheden ved profylaksedosis >4500 IE og den mig bekendt ikke eksisterende evidens bag d-dimer styret (fysiologi-argumenteret) LMWH dosering.
Ref: https://www.stemlynsblog.org/jc-thromboprophylaxis-in-covid-19-patients-st-emlyns/ + https://www.thennt.com/review-covid-analysis-2020/
Case fortsættelse: CT af lungerne på din patient viser ingen LE,, men udbredte C19 forandringer (“Crazy paving”). LMWH 4500 IE gives x1 per dag. Ved udskrivelse skal patienten have eliquis i 3-6 uger
Anti-inflammatorisk behandling
Har patienten nået den inflammatoriske fase (blodprøvemæssigt tegn med stigning i CRP og øvrige fasereaktanter), og er patienten indlæggelseskrævende til iltbehandling, vil vi ofte starte patienten i
- Bethametasone (betapred) 6 mg x1 per dag i 7-10 dage (højere dosis og varighed kan komme på tale ved intensiv patienter)
Efterhånden som der er kommet mere evidens bag Tocilizumab anvendes dette i supplement med bethametasone til udvalgte patienter (udvalgte fordi: dyrt og højere risikoprofil)
- Tocilizumab (RoActemra) 162 mg IM x1 per uge (ofte kun x1 i forløbet)
Ref: TheNNT (https://www.thennt.com/review-covid-analysis-2020/ )
Case fortsættelse: Du indsætter din patient på 6 mg betapred x1 i 7 dage fra akutmodtagelsen , da hun er hyperinflammatorisk. Du giver dog også antibiotika dække da CRP og prokalcitonin på dag 6 giver mistanke om bakteriel infektion i tillæg til C19.
Anti-viral behandling
Ingen tegn til at der findes nogen patient-vigtig og reproducerbar effekt af nogen form for antiviral terapi. På mit hospital anvendes remdisivir (og indtil for nyligt convalescent plasma) af vores infektionslæger, ud fra et rationalistisk argument om at det potentielt kan virke ved patienter med høj viral load.
Studierne på området vidner dog om noget andet, og jeg påminder om problemet med det rationalistiske argument fremsat af mange, herunder Jerome Hoffman i ”…but it makes sense physiologically” eller Justin Morgenstern i ”EBM i still the best kind of medicine”
Ref: TheNNT (https://www.thennt.com/review-covid-analysis-2020/ )
Case fortsættelse: Selv hvis der var nogen vigtig effekt af overstående lægemidler, er patienten udover den virale fase, og du opstarter ikke disse.
Øvrig (vigtig) behandling
- Smertestillende / febernedsættende: Panodil og evt morfin / movikol (NSAID undgås som udgangspunkt pga LMWH)
- Behandlingsbegrænsnings-samtale: For hjælp til dette, se vitaltalks (og bogen af teamet: Mastering communication with seriously ill patients), akutmedicineren (kommunikation del 2 og geriatrisk akutmedicin del 2), EmCases Ep 70 (https://emergencymedicinecases.com/end-of-life-care-in-emergency-medicine/ ), EmCrits podcasts- og SMACC forelæsninger med Ashley Shreves
- Angst: Som ved alle tilstande med lufthunger tolererer nogle det bedre end andre. Ængstelige patienter har svært at kooperere, tager overfladiske åndedræt og/eller hyperventilerer. Kommunikation, ro og evt let sedering kan være nødvendig. På intensivafdelingerne anvendes Dexmedetomidine ofte
- PPI: Kan overvejes som profylakse (særligt ved tidligere ulcus eller ulcus inducerende medicin fx ASA, NOAK, SSRI, prednisolon m.m)
- Proning og positionering: Positionering er altid vigtig, men proning anvendes særligt ved de inflammatoriske NHF og NIV patienter
- Antibiotika og gennemdyrkning: ved mistanke
- Væskebehandling: patienterne er ofte dehydreret initielt (fordi de ikke har kunnet spise og drikke). I starten af pandemien sagde man, at patienten skulle holdes tør, men efterhånden virker det til (= ej evidens), at vi ikke ser overhydrering så ofte. Giv dem væsken de behøver på akutmodtagelsen, og hold dem på den neutrale til tørre side under indlæggelsen
- Medicingennemgang mhp fx AKI, delir risiko lægemidler (se geriatrisk akutmedicin del 1 for detaljr) m.m
Case fortsættelse: Du opstarter din patient i 1g Alvedon x4, Morfin 2,5 mg IV p.n pga takypnø og mistanke om overfladisk vejrtrækning og smerter, gennemdyrker og opstarter i husets vin (som i Region Stockholm – lidt mærkeligt synes jeg – er cefotaxim 1g x3), Giver 1 L Ringer-Acetat i PVK’en til langsomt indløb i tillæg til det patinten kan drikke p.o (hun nævnte hun var tørstig = behov for væske). Ingen behov for medicingennemgang eller behandlingsbegrænsning. Patienten prones ikke, da hun lige nu er stabil i den position hun sidder.
Følg med i del 2 kaldet “Covid, antifragilitet og compassionate care: En genfødsel?”, for en gennemgang af de mere filosofiske- og psykiske elementer af det vi laver (også under Corona), og hvordan vi skaber mening med det.
Referencer om triagering, og for et mere nuanceret blik på triagering:
- WTBS 14 Improving Patient Flow in the ED: 7 Strategies for Nurses (https://emergencymedicinecases.com/improving-patient-flow-ed-7-strategies-nurses/ )
- WTBS 7 – is triage obsolete (https://emergencymedicinecases.com/is-triage-obsolete/ )
- WTBS 6 – Measuring Quality (https://emergencymedicinecases.com/measuring-quality-the-value-of-health-care-metrics/ )
- WTBS 4+5 – Emergency Physician Speed part 1+2 (https://emergencymedicinecases.com/emergency-physician-speed-and-productivity-solutions/ + https://emergencymedicinecases.com/emergency-physician-speed-how-fast-is-fast-enough/ )
- EmCases Ep 129 (Crowding)
- Campell: strategies to managing ED flow
- Iona Heath : Arm in arm with righteousness
- Fatovich : The inverted time curve
- Keijzers : Don’t just do something, stand there
- St Emlyns blog: Only a game? Infinite game theory in Emergency Medicine (https://www.stemlynsblog.org/only-a-game-infinite-game-theory-in-emergency-medicine/ )
- Braithwaite BMJ podcast og artikel: Changing how we think about healtchare improvements
- Braithwaite et al: Selling Patients

