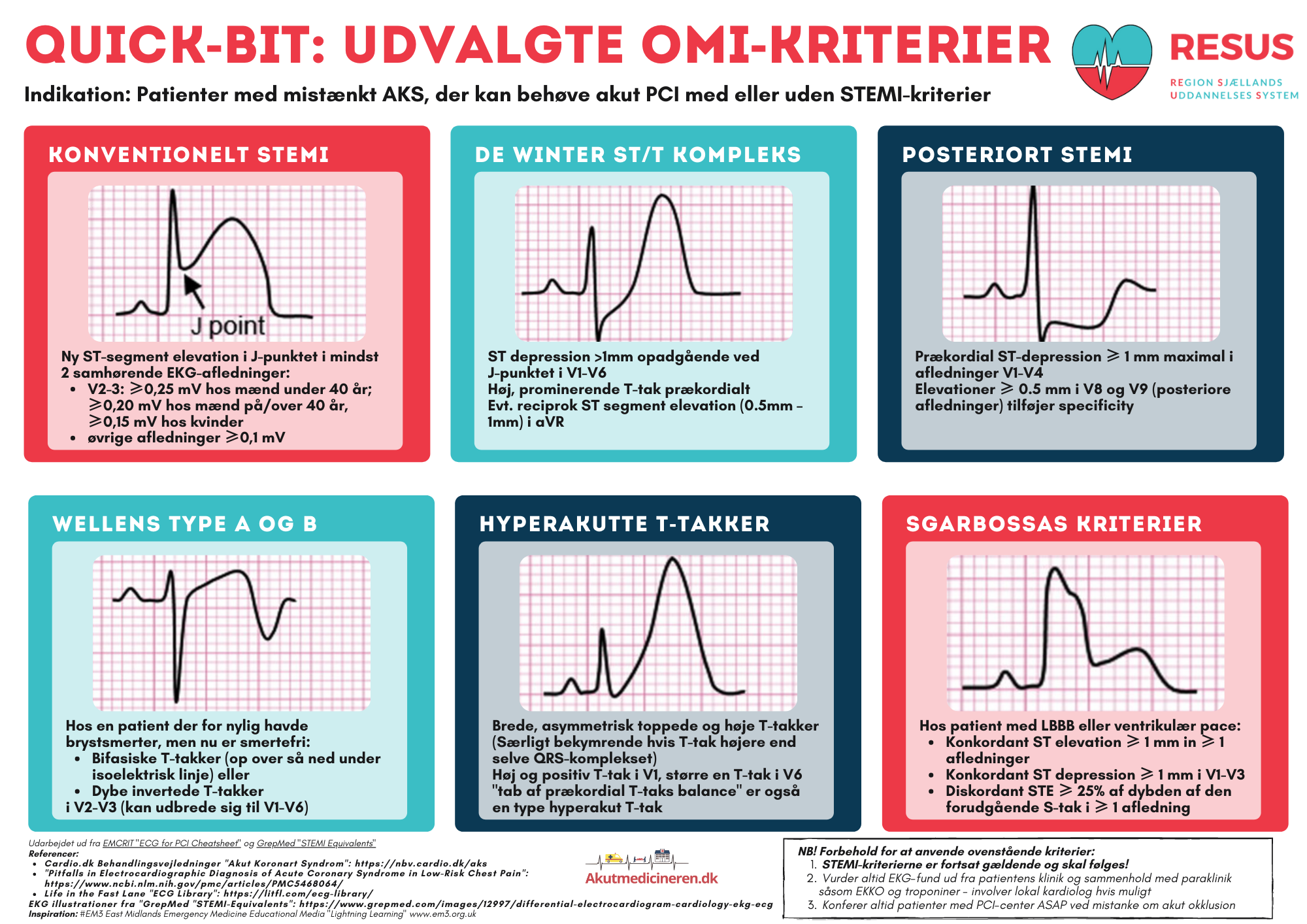
RESUS - Men hvad betyder det?
Kritisk gennemgang af litteratur med fokus på klinisk anvendelighed og hvilke faldgruber vi skal passe på når vi overfører resultaterne til vores egne patienter

"Men hvad betyder det?" er en del af den nye struktur på RESUS-platformen, som kommer til at udgøres af 4 tilbagevendende indlægstyper med udgivelse hver 2. måned:
- "Men hvad betyder det?": Kritisk gennemgang af nye og akutmedicinsk relevante studier ud fra RESUS-tjeklisterne
- "Sådan gør de altså i Amerika": Teoretisk gennemgang af et afgrænset emne ud fra kapitler i Tintinalli's og Rosen's Emergency Medicine
- "Det kan jeg da også godt, det der...": Gennemgang af akutmedicinske procedurer ud fra en struktureret og patientsikker tilgang
- "Det du ikke lærte i skolen": Samtaler om human factors og ikke-tekniske færdigheder indenfor det akutmedicinske speciale
"Men hvad betyder det?" er videreførelsen af de tidligere podcasts på RESUS-platformen, hvor vi dykkede helt ned i kødet på et enkelt studie og brugte en hel podcast på at findissekere de enkelte dele af metoderne og de bias og faldgruber det uundgåeligt leder til. Bygget på den feedback vi taknemmeligt har taget imod forsøger vi nu at nå igennem lidt flere studier, med den konsekvens at vi ikke når helt lige så dybt i det enkelte studie, men vi bevarer fortsat den strukturerede kritiske tilgang til artiklerne ved at anvende tjeklisterne i vores egen gennemgang af studierne. Præsentationen af studierne her i podcast- og blogserien vil derfor være et udtræk af det bedste og det vigtigste fra den gennemgang.
I denne første pilotoptagelse af "Men hvad betyder det?" er introlæge fra Køge Akutafdeling, Emilie Fraisse, med i studiet og vi gennemgår i fællesskab fire studier der dækker bredt over flere emner:
- Konservativ vs. invasiv behandling af lukkede, displacerede humerusskaftsfrakturer
- Røntgenkontrasts association med nyreskade hos patienter mistænkt for LE
- Modificerede Sgarbossa kriteriers præcision i diagnosen af AKS ved pacet rytme
- Effekten af trombolyse hos patienter med intermediær risiko LE
Vi håber at I vil tage godt imod den nye struktur og komme med feedback i kommentarfeltet her på siden eller direkte til akutmedicineren@gmail.com
Podcast optaget den 16/3-22 - Skriftligt resume skrevet af Emil Ejersbo Iversen, marts 2022
Citér denne podcast som:
Iversen, E, Fraisse, E. RESUS - Men hvad betyder det? - Del 1. RESUS, Region Sjællands UddannelsesSystem, Marts 2022. www.akutmedicineren.dk/resus/. Tilgået [dato]
1. studie:
2020 Rämo et al. “Effect of surgery vs. functional bracing on functional outcome among patients with closed displaced humeral shaft fractures: The FISH randomized clinical trial” - JAMA
Overblik:
Randomiseret, kontrolleret studie over effekten af konservativ behandling vs kirurgisk intervention for lukkede, displacerede humerusskaftsfrakturer, foretaget på 2 finske universitetshospitaler i perioden november 2012 til januar 2018
- Patienter blev randomiseret til enten kirurgi eller konventionel konservativ behandling med sarmiento-bandage ved hjælp af "sealed envelope" teknikken
- Begge grupper fik fysioterapi i standardiseret regime
- Patienter der afslog randomisering inviteredes til et observationelt substudie hvor de blev fulgt med den behandling patienterne foretrak (33 konservativ vs 9 kirurgisk intervention)
Population:
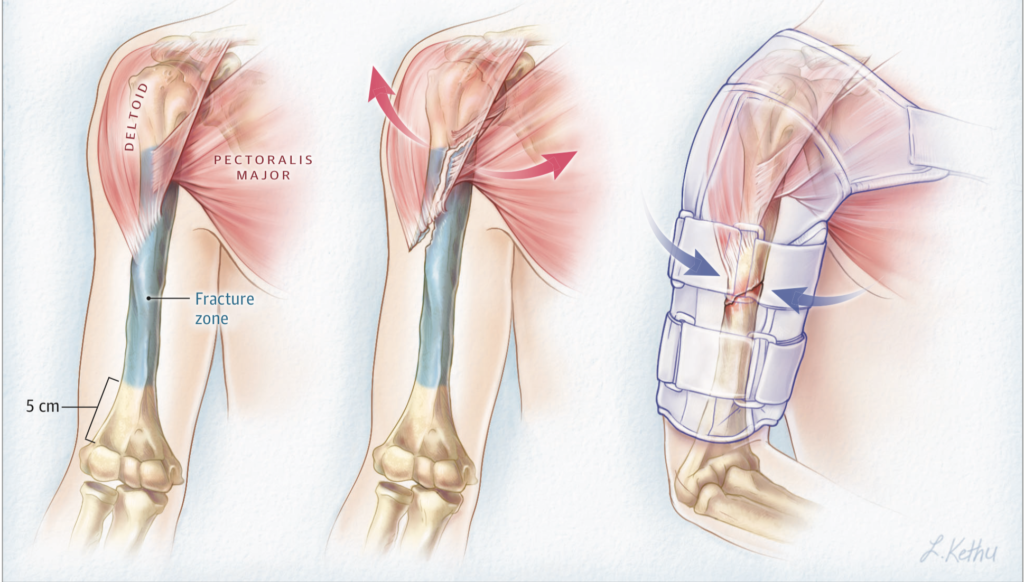
Selvom studiet havde brede inklusionskriterier (patienter >18 år med lukket, displaceret humerusskaftsfraktur) var eksklusionskriterierne forholdsvist skarpe og ekskluderede bl.a. svær komorbiditet, frakturer udenfor den etablerede frakturzone (fra øverste insertion af pectoralis major til 5 cm over fossa olecranon) samt patienter som kognitivt ikke ville kunne medvirke til genoptræning i konservativt regime.
- Ud af kun 321 screenede patienter i løbet af den 6 årige studieperiode blev kun 82 randomiseret. 53 patienter afslog randomisering og indgik i det observationelle studie.
- 181 patienter blev ekskluderet (91 grundet fraktur udenfor det angivne område, 30 grundet svær komorbiditet, 30 grundet kognitive deficit og en række mindre eksklusionsgrupper)
- Kun 2 patienter blev tabt til follow-up i hver af de to randomiserede grupper
Intervention/exposure:
Kirurgi med åben reduction og fixation med plade og skruer og rehabiliteringsprotokol i form af øvelser
- 13 patienter randomiseret til konservativ behandling blev behandlet med kirurgi i løbet af studiets 12 måneders opfølgningsperiode, men blev analyseret i deres oprindeligt tildelte gruppe
- Operationen blev udført enten af eller under supervision af en erfaren ortopædkirurg indenfor 14 dage fra skadetidspunktet
- Patienterne blev instrueret i at de måtte anvende armen umiddelbart efter operationen, men skulle undgå tunge løft i 6 uger
Comparison:
Konservativ behandling med Sarmientobandage og rehabilitationsprotokol i form af øvelser
- Sarmientobandagen blev anlagt af erfaren bandagist og sikrede fri bevægelse af både skulder- og albueled
- Patienterne blev medgivet mundtlig og skriftlig information om bandagepleje
- Genoptræningen fulgte et standardiseret forløb udviklet på baggrund af den oprindelig Sarmiento-metode med svingbevægelser uden vægt umiddelbart efter anlæggelse af bandage, passive skulderøvelser fra 3 uger og vægtbærende øvelser fra 6 uger
Outcome:
Primære: Funktion målt på DASH-scoren (patientrapporteret) efter 12 måneder
Sekundære: Smerter i hvile og ved aktivitet, Constant-Murley score (subjektiv og objektiv funktionsmåling) samt andre standardiserede skalaer og generel patienttilfredsstillelsesscore målt på Likert skala
- Data blev indsamlet for studiets primære outcome ved baseline, efter 6 uger og efter 3, 6 og 12 måneder ifb. med kliniske opfølgninger
- Patienternes randomisering blev forsøgt blændet bedst muligt overfor klinikerne ved at patienterne blev bedt om at bære langærmede t-shirts som ikke måtte fjernes
- Data om komplikationer blev indsamlet af et medlem af forskergruppen som ikke havde været involveret i patienternes oprindelige behandling og blev delt ind i mindre og alvorlige komplikationer
Hvad fandt de ud af?
Studiet fandt ingen signifikant forskel i funktionelt outcome målt på DASH-skalaen efter 12 måneder. Patienterne i kirurgigruppen opnåede dog hurtigere en bedre funktion, særligt i de første 3 måneder og 11 af patienterne fra den konservative gruppe udviklede nonunion mens i alt 13 patienter fra den konservative gruppe måtte undergå kirurgi indenfor de 12 måneder studiet forløb over. Der fandtes heller ingen signifikante forskelle i studiets sekundære outcomes.
Hvad betyder det?
Dette lille, men ganske veludførte randomiserede kontrollerede studie finder ingen signifikant forskel i funktionelt outcome 12 måneder efter lukket, displaceret humerusskaftsfraktur behandlet enten konservativt med sarmientobandage og fysioterapi eller kirurgisk med plade og skruer samt fysioterapi.
Selvom studiet fandt en signifikant bedring i funktionelt outcome indenfor de første 3 måneder hos patienter behandlet kirurgisk, udlignedes denne forskel efter ca 6 måneder og grupperne var helt sammenlignelige efter 12 måneder. Dog blev 13 ud af de 44 patienter i den konservative kontrolgruppe opereret i løbet af de 12 måneder grundet non-union, men analyseret i deres intention-to-treat analyse, hvilket kan have skævvredet resultaterne til fordel for konservativ behandling.
Studiet fandt ingen signifikant forskel i komplikationer, men den lille population på 82 patienter gør det usandsynligt at studiet har haft power til at detektere en signifikant forskel.
Trods dette er selve udførelsen af randomiseringen og blændingen særlige styrker for studiet, hvilket bestyrker tiltroen til resultaterne. De primære kritikpunkter falder på en formodet manglende fortløbende inklusion (studiet løber over 6 år, men screener kun 321 patienter på to store universitetshospitaler, hvilket giver mistanke om sampling bias), en betydende crossover samt manglende information omkring standardisering af andre regimer, såsom smertestillende, hvilket formentligt særligt vil have kunnet påvirke evnen til at medvirke til fysioterapi i gruppen der blev behandlet konservativt.
Hvad fortæller jeg min patient?
"Ud fra dette studie synes funktionen af armen at være fuldstændigt ens efter 12 måneder uafhængigt om du bliver behandlet kirurgisk eller konservativt for dit overarmsbrud. Der er set en hurtigere rehabilitering og tilbagevenden til nær fuld funktion ca. dobbelt så hurtigt blandt patienter der bliver opereret og en del af de patienter der ikke bliver opereret oplever at knoglen ikke vokser ordentligt sammen og må opereres efterfølgende. Enhver operation indebærer selvfølgelig risici, men selvom dette studie ikke viste en signifikant forskel mangler vi robust evidens for den egentlige risiko for komplikationer ved dette indgreb.
Det er forskelligt fra person til person om den hurtigere funktionsbedring er risikoen ved en operation værd. Vi sætter din arm i bandage, giver dig smertestillende og henviser dig til en subakut tid i ortopædkirurgisk ambulatorium, hvor du sammen med ortopædkirurgen vil kunne træffe beslutning omkring hvilken behandling der er bedst i dit specifikke tilfælde."
2. studie:
2021 Goulden et al. “Association of intravenous radiocontrast with kidney function: A regression discontinuity analysis” – Jama Internal Medicine
Overblik:
Observationelt kohortestudie der anvender en teknik kaldet “fussy regression discontinuity” til at vurdere graden af nyrepåvirkning efter IV kontrast i forbindelse med CT lungeemboli sammenlignet med patienter der ikke blev udsat for kontrasten.
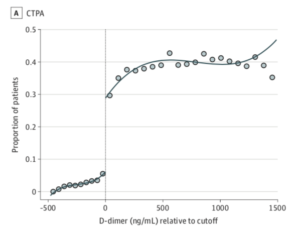
Metoden der anvendes udnytter det faktum at der på baggrund af måling af D-dimer og den fastsatte cut-off værdi opstår en ”kunstig”, men ganske betydelig forskel i sandsynligheden for at blive udsat for kontrast ifb. med en scanning for lungeemboli. Ved at kigge på de patienter der ligger hhv. lige over og lige under cut-off værdien for D-dimer opnår studiet både en ”case” og ”kontrol” kohorte, med et meget stort spring i hvor mange der har modtaget IV kontrast, men som for alle andre praktiske formål burde være sammenlignelige. Er der en association imellem IV kontrast og nedsat nyrefunktion burde der altså være et tilsvarende stort spring i påvirkningen af nyrefunktion efter IV kontrast.
Population:
Patienter >18 år som I perioden 2013-2018 havde fået målt en D-dimer på en af akutafdelingerne i den canadiske provins Alberta
- Eksklusionskriterier: Ingen eGFR målt indenfor 2 timer fra D-dimer, D-dimer lige akkurat på cut-off værdien, dialyse indenfor 6 måneder før inklusion. Kun første besøg blev inkluderet.
Case-kohorte: Patienter lige over cut-off for D-dimer med høj sandsynlighed for at modtage en CT lungeemboli med IV kontrast
Kontrol-kohorte: Patienter lige under cut-off for D-dimer med lavere sandsynlighed for at modtage CT lungeemboli og dermed kontrast.
Intervention/exposure:
Intravenøs kontrast I forbindelse med CT lungeemboli
Comparison:
Ingen kontrast grundet D-dimer under cut-off
Outcome:
Primære: eGFR op til 6 måneder efter udsat for IV kontrast
Sekundære: Behov for dialyse indenfor 6 måneder, akut nyresvigt (defineret som fald i kreatinin >50% eller 26 µmol/L over 7 dage) og død indenfor 6 måneder
Hvad fandt de ud af?
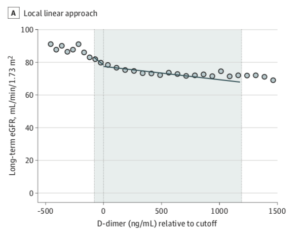
Studiet fandt iblandt de 156028 inkluderede patienter en 23% ”diskontinuitet” (hhv. 5% i gruppen under cut-off vs. 30% i gruppen over) i udsættelse for kontrast, men ingen forskel i eGFR efter 6 måneder med en gennemsnitlig ændring i eGFR på -0,4 mL/min/1,73m2 (CI -4,9 til 4,0) . Studiet fandt ligeledes ingen forskel i behov for dialyse (Risk Difference (RD) 0,07% CI -0,47% til 0,61%), død (RD 0,3% CI -2,9% til 3,2%) eller akut nyresvigt (RD 4,3% CI -2,7% til 12,9%).
Den gennemsnitlige baseline eGFR i studiet var 86, men i subgrupperne med eGFR hhv. over og under 45 fandtes der heller ingen signifikant forskel med en gennemsnitlig ændring på -3,6 mL/min/1,73m2 (CI -9,5 til 1,8) i gruppen med eGFR >45 mod 0,5 mL/min/1,73m2 (CI -12,1 til 33,8) i gruppen med eGFR <45.
Studiet fandt en nær statistisk signifikant, men ikke oplagt klinisk relevant forskel i eGFR i en subgruppe af patienter med diabetes med en gennemsnitlig ændring i eGFR på -6,4mL/min/1,73m2 (CI -15,4 til 0,2). Studiet var dog ikke powered til at detektere en signifikant forskel i denne subgruppe.
Hvad betyder det?
Dette observationelle studie, som ved at anvende den statistiske metode ”diskontinuitets regressions analyse” kraftigt øger sit potentiale til at detektere kausalitet fandt ingen sammenhæng imellem IV kontrast og nyrepåvirkning blandt canadiske patienter der fik taget en D-dimer på akutafdelingen, fraset måske i en subgruppe af patienter med diabetes. Dette ligger i tråd med andre nylige studier, som udfordrer eksistensen af kontrastinduceret nefropati, særligt efter fremkomsten af nyere kontrastmidler og scanningsprotokoller.
Da der trods diskontinuitetsanalysen fortsat er tale om et observationelt studie og ”kun” 30% af patienter med D-dimer lige over cut-off værdien fik kontrast forbliver risikoen for et spektrumbias uændret, idet klinikere i perioden kan have fravalgt kontrastscanning for patienter i højest risiko for nyrepåvirkning i højere grad end ”raske”.
Hvad fortæller jeg min patient?
"Vi er bekymrede for at du kan have en blodprop i lungen, hvilket vi hurtigt kan få afklaret ved at tage en CT-scanning. Scanningen indebærer kontrast og din nyrefunktion er tæt på grænsen for hvornår vi vil give dette, da det tidligere er set at patienter har fået nyrepåvirkning på baggrund af kontrasten. De seneste studier, som er lavet efter at vi har fået nyere og bedre kontrast, som vi kan anvende i mindre doser, tyder dog på at risikoen for nyrepåvirkning er negligeabel og da du ikke har diabetes er du ikke i en særlig risikogruppe. Vi anbefaler derfor at du får foretaget scanningen, så vi kan give dig den rigtige behandling såfremt vi finder en blodprop. Havde du haft en væsentligt dårligere nyrefunktion kunne vi have været nødt til at foretage scanningen uden kontrast."
3. studie:
2021 Dodd et al. “Electrocardiographic diagnosis of acute coronary occlusion myocardial infarction in ventricular paced rhythm using the modified Sgarbossa criteria” – Annals of Emergency Medicine
Overblik:
Retrospektivt case-kontrol studie over præcisionen af de modificerede Sgarbossa-kriterier vs. de originale i diagnostikken af okklusionsmyokardieinfarkt (OMI) hos patienter med ventrikulærpacet hjerterytme på EKG og symptomer på AKS.
Det var i mange år overbevisningen at patienter med venstresidigt grenblok eller ventrikulær pacet rytme ikke kunne få diagnosticeret AKS ud fra EKG forandringer, da de to tilstande kan medføre påvirkning af både Q-tak udvikling og ST-morfologien, hvilket gør traditionelle STEMI/NSTEMI kriterier ubrugelige. I nyere tid har guidelines fra bl.a. American College og Cardiology anbefalet anvendelsen af Sgarbossa kriterierne i diagnosticeringen af patienter med symptomer på AKS og venstresidigt grenblok eller ventrikulær pacet rytme. De originale Sgarbossa kriterier har dog en meget lav sensitivitet, primært grundet fortsat brug af absolutte værdier, såsom 5mm elevation, hvorfor de siden er blevet modificerede af bl.a. FOAMed EKG-eksperten Stephen W. Smith, til at omfatte relative ændringer i EKG’ets morfologi.
Population:
Ptt. >18 år med symptomer på AKS og ventrikulær pacet rytme på EKG som præsenterede sig til en af 16 internationale akutafdelinger eller primære PCI centre i perioden januar 2008-2018.
- Eksklusionskriterier: Fravær af symptomer ved EKG optagelse, manglende ventrikulærpacet rytme, puls >130, dBT >120, lungeødem krævende CPAP, K+ >5,5
Case-kohorte: Patienter der opfyldte inklusionskriterier og undergik angiografi med fund af OMI i perioden januar 2008 til januar 2018
Kontrol-kohorte: Patienter der opfyldte inklusionskriterier og undergik angiografi uden fund af OMI samt tilfældig kohorte af patienter der opfyldte inklusionskriterier fra akutafdelingen uden AKS (ingen tegn på myokardieskade eller vurderet oplagt type 2 infarkt).
Indekstest:
Modificerede Sgarbossa kriterier (+V4-V6)
- Konkordant ST-segment elevation >1mm eller
- Konkordant ST-segment depression >1mm i V1-V6 eller
- Diskordant ST-segment elevation med ST/S ratio >25%
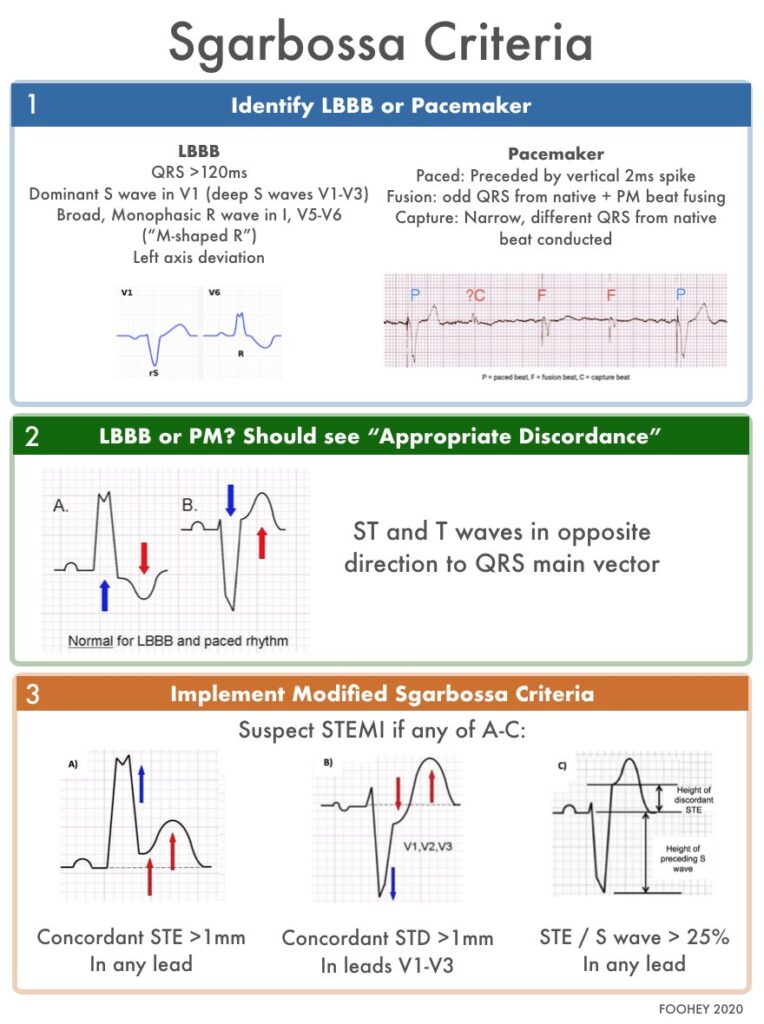
Comparison:
Originale Sgarbossa kriterier
- Konkordant ST-segment elevation >1mm eller
- Konkordant ST-segment depression >1mm i V1-V3 eller
- Diskordant ST-segment elevation >5mm
Target condition:
Okklusionsmyokardieinfarkt (OMI) defineret som angiografi med TIMI flow 0-1 eller TIMI 2-3 med intervention og højt troponinudslip
Referencestandard:
Angiografi vurderet af uafhængige, blændede interventionskardiologer sammenholdt med højeste troponinudslip.
Hvad fandt de ud af?
Sensitiviteten for de modificerede Sgarbossa kriterier var væsentligt højere end de originale på hhv. 86% (CI 69 til 90) vs. 56% (CI 42 til 69). Set alene fandt diskordans kriteriet (ST/S ratio >25%) i de modificerede Sgarbossa kriterier 15 ekstra OMI sammenlignet med de originale (>5mm).
Specificiteten var bevaret høj på hhv. 96% (CI 90 til 99) for de modificerede kriterier vs. 97% (CI 92 til 99) for de originale. LR+ var høj på hhv. 21 for de modificerede og 19 for de originale kriterier. Forventeligt var der stor forskel på LR- som var hhv. 0,19 for de modificerede og 0,45 for de originale kriterier.
Hvad betyder det?
Dette retrospektive case-kontrol studie finder en forbedret sensitivitet og bevaret specificitet i diagnostikken af OMI hos patienter med ventrikulærpacet rytme ved anvendelse af de modificerede Sgarbossa kriterier fremfor de originale. Den lave incidens af ventrikulærpacet rytme nødvendiggjorde det retrospektive design (hvilket understreges af at der på 16 centre over 10 år kun blev fundet 56 case-patienter), hvilket er studiets største svaghed.
Andre faldgruber er dog også potentiel eksklusion af de sygeste patienter gennem fysiologiske eksklusionskriterier samt et potentielt bias i form af at ikke alle kontrolpatienter gennemgik angiografi.
Trods disse mangler og faldgruber understreger studiet dog anvendeligheden af særligt de modificerede Sgarbossa kriterier hos patienter med ventrikulær pacemaker, som trods de udgør en relativt lille andel af patienter der præsenterer sig med brystsmerter i akutafdelingen (ca 2,5%) historisk har haft højere risiko for fejldiagnose og overset AKS samt øget mortalitet grundet manglen på validerede EKG-fund der med pålideligt kunne diagnosticere frisk okklusion, ligesom patienter med venstresidigt grenblok.
Hvad fortæller jeg min patient?
"Din pacemaker betyder at vi ikke kan anvende de normale fund på hjertekardiogrammet der gør os i stand til med høj sandsynlighed at sige at der er tale om en akut blodprop i dit hjerte som årsag til dine symptomer. Dit hjertekardiogram har dog nogle tegn der kan pege i retning af at det alligevel er det der er tale om og sammenholdt med dine symptomer vurderer vi at det er bedst at lave en hurtig undersøgelse hvor vi ved at gå ind igennem blodåren i håndleddet kan direkte visualisere en evt. blodprop og i samme instans behandle den."
4. studie:
2014 Meyer et al. “Fibrinolysis for patients with intermediate-risk pulmonary embolism” – New England Journal of Medicine
Overblik:
Randomiseret, kontrolleret, dobbeltblændet multicenterstudie over effekten af trombolyse + heparin vs. placebo + heparin på hæmodynamisk dekompensation og død hos patienter med intermediær-risiko lungeemboli, defineret som højresidig belastning + troponinudslip, men hæmodynamisk stabile. Patienter blev via en central algoritme randomiseret i klynger indenfor 2 timer efter konstateret lungeemboli med intermediær risiko
Population:
Fra november 2007 til juli 2012 blev 1006 patienter registreret som deltagende i PEITHO studiet fordelt på 76 lokationer i 13 lande.
- Inklusionskriterier: >18 år, bekræftet LE med symptomdebut indenfor 15 dage, højresidig belastning på EKKO eller CT og troponinudslip
- Eksklusionskriterier: Hæmodynamisk kollaps ved inklusion, kendt blødningsrisiko, tidligere trombolyse indenfor 4 dage, sBT >180 eller dBT >110 ved randomisering, kendt allergi, gravid, vurderet i for høj risiko af forsker.
- 506 patienter randomiseret til interventionsgruppen og 500 til placebogruppen
- 1 patient tabt til follow-up (manglende samtykkeerklæring)
Intervention/exposure:
Trombolyse i form af bolus tenecteplase i vægtafhængig dosis
- Interventionsgruppen blev givet en enkelt bolus tenecteplase over 5-10 sekunder + ufraktioneret heparin mens placebogruppen fik en ækvivalent volumen væske af samme udseende som tenecteplasen over 5-10 sekunder + ufraktioneret heparin.
- 5 patienter fik ikke den i randomiseringen tildelte intervention, men alle analyser blev udført som intention-to-treat
Comparison:
Placebo I form af unavngivet væske i samme volumen og udseende som tenecteplasen
- Alle inkluderede patienter blev givet ufraktioneret heparin i form af initial bolus efterfulgt af infusion styret efter aPTT 2-2,5x normalgrænsen
Outcome:
Primære outcome:
Sammensat outcome af død eller hæmodynamisk dekompensering/kollaps indenfor 7 dage efter randomisering.
- Definitionen af hæmodynamisk kollaps omfattede alt fra et isoleret, vedvarende fald i blodtryk til behov for genoplivning.
Sikkerheds outcomes:
Iskæmisk eller hæmoragisk stroke indenfor 7 dage efter randomisering, større ekstrakraniel blødning indenfor 7 dage efter randomisering samt alvorlige hændelser indenfor 30 dage efter randomisering.
Sekundære outcomes:
Hhv. død, hæmodynamisk kollaps og symptomgivende re-trombosering indenfor 7 dage efter randomisering samt død indenfor 30 dage efter randomisering.
Hvad fandt de ud af?
Det primære outcome, sammensat af død eller hæmodynamisk kollaps, fandt sted indenfor 7 dage efter randomiseringen hos 13 (2,6%) af patienter i interventionsgruppen mod 28 (5,6%) i placebogruppen med en OR på 0,44 (CI 0,23-0,87 p= 0,02). Dog var det kun hhv. 6 (1,6%) ptt. i interventionsgruppen og 9 (1,8%) patienter i placebogruppen der døde (p=0,42), mens resten oplevede forskellige grader af hæmodynamisk kollaps (kun hhv. 1 og 5 patienter i de to grupper krævede genoplivning).
23 (4,6%) af patienterne i placebogruppen og 4 (0,8%) i interventionsgruppen fik fibrinolyse udover den i studiet tildelte intervention. Heraf fik 9 patienter fibrinolyse inden den egentlige intervention var givet.
Efter 30 dage var 12 patienter (2,4%) i interventionsgruppen mod 16 (3,2%) i placebogruppen (p=0,42) døde.
Indenfor 7 dage fra randomiseringen oplevede 32 patienter (6,3%) i interventionsgruppen større ekstrakraniel blødning mod 6 patienter (1,2%) i placebogruppen. 12 patienter (2,4%) i interventionsgruppen fik stroke, heraf 10 hæmorragiske, mod kun 1 i placebogruppen (p=0,003).
Hvad betyder det?
Dette meget veludførte randomiserede, kontrollerede, dobbeltblændede multicenterstudie udført på 1006 patienter med et imponerende lavt frafald på 1 og crossover på 23 viste en signifikant nedsat forekomst af det sammensatte outcome død eller hæmodynamisk kollaps indenfor 7 dage ved behandling af patienter med lungeemboli med intermediær risiko (defineret som hæmodynamisk intakt, men med højresidig belastning og troponinudslip) med fibrinolyse i form af tenecteplase + ufraktioneret heparin sammenlignet med placebo + ufraktioneret heparin med en OR på 0,44. Den statistiske signifikans forsvandt dog når der kun blev kigget på død, som forekom hos et fåtal af patienterne. Studiet formåede desuden at vise en signifikant forøget forekomst af større ekstrakraniel blødning og stroke i fibrinolysgruppen.
Den umiddelbart imponerende OR for det sammensatte outcome blegner dog lidt når tallene konverteres til et number-needed-to-treat (NNT) på 33,3 mod et number-needed-to-harm på 19,6 for stroke og NNH 11 hvis større ekstrakraniel blødning tælles med.
Hvad fortæller jeg min patient?
"Den blodprop du har i lungen, som forårsager dine symptomer, er alvorlig og kræver behandling med blodfortyndende medicin. For nu har du dog et normalt blodtryk, hvilket tyder på at dit hjerte, trods at vi kan se at det er belastet af blodproppen, kan opretholde sin funktion. Den bedste viden vi har tilgængelig tyder derfor på at vi, for at afveje behovet for at behandle din blodprop med risikoen for at du får en større blødning, for nu ikke bør give dig det kraftigste blodfortyndende medicin, men i stedet noget der stadig fortynder blodet og har en god chance for at opløse blodproppen, men har en mindre risiko for at forårsage blødning andre steder. Skulle du blive mere alvorligt syg kan vi dog blive nødt til at give den kraftigt blodfortyndende på et senere tidspunkt."
Referencer og mere FOAMed om emnerne:
- Rämö L, Sumrein BO, Lepola V, Lähdeoja T, Ranstam J, Paavola M, Järvinen T, Taimela S; FISH Investigators. Effect of Surgery vs Functional Bracing on Functional Outcome Among Patients With Closed Displaced Humeral Shaft Fractures: The FISH Randomized Clinical Trial. JAMA. 2020 May 12;323(18):1792-1801. doi: 10.1001/jama.2020.3182. PMID: 32396179; PMCID: PMC7218498.
- Goulden R, Rowe BH, Abrahamowicz M, Strumpf E, Tamblyn R. Association of Intravenous Radiocontrast With Kidney Function: A Regression Discontinuity Analysis. JAMA Intern Med. 2021 Jun 1;181(6):767-774. doi: 10.1001/jamainternmed.2021.0916. PMID: 33818606; PMCID: PMC8022267.
- Dodd KW, Zvosec DL, Hart MA, Glass G 3rd, Bannister LE, Body RM, Boggust BA, Brady WJ, Chang AM, Cullen L, Gómez-Vicente R, Huis In 't Veld MA, Karim RM, Meyers HP 3rd, Miranda DF, Mitchell GJ, Reynard C, Rice C, Salverda BJ, Stellpflug SJ, Tolia VM, Walsh BM, White JL, Smith SW; PERFECT study investigators (the complete list of PERFECT study investigators is provided in Appendix E1, available at http://www.annemergmed.com). Electrocardiographic Diagnosis of Acute Coronary Occlusion Myocardial Infarction in Ventricular Paced Rhythm Using the Modified Sgarbossa Criteria. Ann Emerg Med. 2021 Oct;78(4):517-529. doi: 10.1016/j.annemergmed.2021.03.036. Epub 2021 Jun 23. PMID: 34172301.
- Meyer G, Vicaut E, Danays T, Agnelli G, Becattini C, Beyer-Westendorf J, Bluhmki E, Bouvaist H, Brenner B, Couturaud F, Dellas C, Empen K, Franca A, Galiè N, Geibel A, Goldhaber SZ, Jimenez D, Kozak M, Kupatt C, Kucher N, Lang IM, Lankeit M, Meneveau N, Pacouret G, Palazzini M, Petris A, Pruszczyk P, Rugolotto M, Salvi A, Schellong S, Sebbane M, Sobkowicz B, Stefanovic BS, Thiele H, Torbicki A, Verschuren F, Konstantinides SV; PEITHO Investigators. Fibrinolysis for patients with intermediate-risk pulmonary embolism. N Engl J Med. 2014 Apr 10;370(15):1402-11. doi: 10.1056/NEJMoa1302097. PMID: 24716681.
- Anand Swaminathan, "The FISH RCT: Surgical vs Non-Surgical Management of Displaced Humeral Shaft Fractures", REBEL EM blog, June 1, 2020. Available at: https://rebelem.com/the-fish-rct-surgical-vs-non-surgical-management-of-displaced-humeral-shaft-fractures/.
- Morgenstern, J. Does contrast cause kidney injury? The evidence, First10EM, November 21, 2017. Available at:
https://doi.org/10.51684/FIRS.4928 - RCEM Learning October 2021, New in EM, utility of modified sgarbossa criteria for OMI. https://www.rcemlearning.co.uk/foamed/october-2021/
- EMDocs: Controversies of thrombolytics for pulmonary embolism. http://www.emdocs.net/controversies-of-thrombolytics-for-pulmonary-embolism/