“All things considered, about this life prolonging treatment
Uddrag fra samtale med 96 årig mand fra Hanson et al, 2019: What matters at the end of life
and that accounts for the hospitals as well.
I don’t wish this
to prolong life
It’s just a good life that comes to an end.”
When he was asked, whether the fear of losing the ability
of taking care of himself was a reason for the abovementioned
statement and therefore greater than the fear
of dying, the answer was “absolutely.”
Hvorfor tage samtalen?
Sjældent er svaret på dette spørgsmål besvaret bedre end i denne fantastiske gratis artikel fra region syddanmark / OUH-holdet indenfor akutmedicin af Stine Hanson, Mikkel Brabrand, Anne-marie Lassen, Jesper Ryg og Dorthe Nielsen: What matters at the end of life
De fleste ældre patienter har gjort sig tanker om behandlingsniveau, inden de ankommer til hospitalet. De har desuden også lyst til at tale om dette emne, også i akutmodtagelsen (særligt om HLR-delen). Faktisk forventes det ofte, og skaber frustration, når vi undlader
“I don’t understand, why you just don’t cut out something
Uddrag om frustrationen fra ægtefælde, der har måtte se sin kone indlagt flere gange. Fra Hanson et al, 2019: What matters at the end of life
like that [standard questions] [red: fx allergier, tidligere, medicin, rygning] and asks about what is really relevant [refers to EOL questions]”
Dette skal dog gerne være med den rette person (“someone with sense of what’s going on”) og i den rette situation – at finde dette smørhul, kræver, at man stikker følerne ud i ENHVER samtale med ældre (særligt ved multiple indlæggelser, frailty og multisygdom), og siger de nej, må man respektere det (særligt raske ægtefælder der tog sig af handicappede / demente pårørende; religiøse patienter og patienter, der boede på plejehjem var i Hanson et al mindre villige til at tale om det). Om ikke andet, kan et frø være plantet til senere i forløbet, når den rette person og situation opstår. Siger de ja, derimod, kan du få gode råd og hjælp til samtalen i denne blog, og min kommunikationsblogserie

HLR-samtalen – Vi gør det for lidt…
Jeg ville ønske det var anderledes, men jeg føler vi har brug for at tale om hvad vi skal gøre, hvis dit hjerte stopper under indlæggelsen.
Vil det være okay?
Majoriteten af både patienter og sundhedspersonale er over-optimistiske ift chancen for genoplivning efter HLR. I én undersøgelse mente 80% af personer >70 år, at deres chance for overlevelse ved HLR scenarie var >50 %. En stor del af resten mente denne chance var >90% (Ragland et al)
Statistikken på området viser dog et mindre optimistisk billede. Ifl dansk hjertestops statistisk (2001-2016), overlever ca 1/10 OHCA (Out of Hospital Cardiac Arrest). Der generelt i litteraturen har en mere fordelagtig prognose end IHCA (in hospital cardiac arrest). Dette dels pga at patienterne er mere raske udenfor hospitalet, og årsagerne for OHCA oftere har stødbare rytmer (god prognose), og lidelser man kan intervenere på (fx AKS eller Arytmi).
Desværre har meget af den ældre litteratur på området været fokuseret på overlevelse (survival) og ikke overlevelse med godt neurologisk outcome, hvilket i virkeligheden er det patienterne ønsker og mener, når de takker ja til genoplivning. Jeg skrev et systematisk review til min KA opgave i netop dette emne (neuroprognosticering af hjertestopspatienter). Detaljeret gennemgang af emnet må blive en anden gang, men ved samtalen med patienten kan det være godt at have lidt basal viden om emnet, da en del af “ærligheden”, som patienterne ønsker, må bunde i fakta om sandsynligheden for overlevelse- og overlevelse med godt neurologisk outcome. Derfor en kort opsummering af essensen om neurologisk prognose efter hjertestop:
- Den neurologiske prognose er svær at vurdere pga konceptet med self-fulfilling prophecy ifb beslutningen om WLST (Withdrawal of life sustaining therapy) – i.e jeg tror du har et dårligt outcome, derfor slukker jeg respiratoren og giver mig selv ret. Samme problemstilling er illustreret ved HLR scenarier, og man har i England sat fokus på problemet
- Mere sikker prognosticering kræver tæt samarbejde mellem anæstesi og neurologi gennem hele forløbet, da flere tests for prognose skal tages i de første 0-72 timer (hvilket sjældent gennemføres sufficient i min erfaring fra Københavnske og Stockholmske neurologiske afdelinger)
- Neuroprognosticering skal være multimodal (ingen enkelt test kan sikkert sige noget om prognose). Metoderne er som følger i kronologisk rækkefølge fra stærkest til svagest målt på FPR (false-positive rate – hvor ofte er testen falsk-positiv og sender folk unødigt i døden, hvis man afhænger alene af den): Neurofysiologi (FPR <5%), Neurologisk undersøgelse af pupilreflekser (FPR <5%), MR skanning, myklonier første 24 timer, blodprøver fx NSE eller S-100B, CT skanning. De sikreste metoder er desværre sværest af få (neurofysiologi: måling af Somatosensoriske Evoked Potentials (SSEP), og cEEG med særlige mønstre herunder nedsat/fravær at responsiveness, burst-suppression). Årsagen til, at det SKAL være multimodal diagnostik, er fordi ingen af overstående prognostiske værktøjer konsistent har FPR på 0
- Timingen af den konklusive multimodale neuroprognosticeringen sker ofte for tidligt (særligt nu hvor man udfører Targeted Temperature Management aka ”køling”, og sedering ifb køling), og bør tidligst ske efter 72 timer fra ROSC – gerne senere
- Anvendelse af score systemer er ikke implementeret, og stod det til mig, skulle man lave scores på logiske dele af forløbet, vi ved giver dårligere prognose (fx ingen HLR fra start, kvalitet af HLR, ikke-stødbare rytmer, lang ”downtime”, patientens multimorbiditet og frailty score, OHCA Vs IHCA m.m). Detajler fra dansk hjertestopregister 2001-2016 viser, at bevidnet OHCA med størbar rytme og tidlig HLR opnår ROSC i knap 50% og har en 30 dages overlevelse på 30%. Derimod med ikke-bevidnet hjertestop med ikke-stødbar rytme, opnår knap 5% ROSC og der er en 30 dages overlevelse på 0,8%. Begge er langt fra ”gennemsnittet” på 1/10 overlevende ved OHCA.
Med alt dette (særligt problemet med WLST) in mente, så er den bedste statistik for godt neurologisk outcome efter OHCA følgende: Af de der opnår ROSC og indlægges på intensivafsnittet er ca 50-80% komatøse (de ikke komatøse har generelt mere favorabelt outcome). Af de komatøse vil ca 50-66% dø, oftest pga WLST (jf herover). Af dem, der overlever til udskrivelse, har de fleste godt neurologisk outcome (ERC 2015 og Sandroni et al, 2018). Pga problemet med pessimisme har den engelske anæstesiologiske forening gået ud med en skrivelse, hvor de advarer imod for tidlig pessimisme ved bl.a. hjertestopsprognosticering (Harvey et al, 2018). Et kontrasvar til dette er dog en udtalelse fra en tidligere redder, ved adspørgsel om han vil genoplives:
“It is all about timing”
Hanson et al, 2019: What matters at the end of life
If the correct treatment is set in early and the cause of the cardiac arrest is reversible, then the chance of a “good outcome” is much better. That is why my answer is not that simple, he explained,
“Because, if time passes by [before cardiopulmonary
resuscitation is started], then it does not matter anymore. I do not intent to spend the rest of my days being a vegetable”
Et andet evigt argument er også studierne, der viser, at folk med neurologiske skader kan have høj livskvalitet efterfølgende – også selvom de ikke mener de før et hjertestop ville have det (Harvey et al, 2018). Der er dog helt klart nogle, som ikke har det godt – dette viser erfaring fra Italienske og koreanske studier på området (Estraneo, 2013), hvor man af religiøse årsager ikke har lov at beslutte WLST. I disse studier, viser det sig, at personer, der efter uger ikke har tegn til godt outcome neurologisk outcome, sjældent får det.
Måske man skulle sætte en grænse på – hvis man ikke genoplives indenfor 5 minutter, så stopper man?
…mit hoved snurrer
Ja, det kan jeg godt forstå! – og prøv du at forklare den 80 årige delirøse patient om alt det, inden hun kører op på afdelingen!
Selvom studierne herover generelt er lavet på yngre patienter med OHCA, så er statistikken på ældre ikke nødvendigvis mere pessimistisk. Et systematisk review af 415.000 patienter > 70 år, viste, at 40% med IHCA opnår ROSC, og halvdelen overlevede til udskrivelse – ikke dårligt når gennemsnitlig OHCA overlevelsen i Danmark er 1/10. Det roder også lidt med vores antagelse af, at OHCA overlever oftere end IHCA. Flere studier viser lignende i aldersgrupper >70 med lille forværring >85 år (Nickels et al).
Alder ALENE er
derfor ikke et godt mål
for om prognosen efter HLR er god eller eji
I stedet skal vi gå til konceptet om frailty igen. Statistikken på patienten med frailty viser nemlig betydeligt dårligere outcome: Kun 5-6% har 30 dages overlevelse (obs WLST), og kun 1,1% har favorabel neurologisk outcome (Nickel et al og Sulzgruber et al, 2017).
…giv mig nu bare et tal!
Okay okay – men jeg prøver bare at forklare kompleksiteten af det her emne, før vi dykker ind i hvad, man kan gøre. Som du nok kan forstå, er der ingen algoritme for det her. Som Hanson og kolleger diskuterer:
“Our findings suggest the need for not “just” a systematic approach in securing EOL preferences, but an approach that is individual and flexible. The individuality of when or if an older person changes their EOL wishes could be related to the lived life of the individual, along with their definition of what brings value into their life. These questions might be just as important as the EOL treatment questions”
Hanson et al, 2019: What matters at the end of life
Vi er altså nødt til at grave ind i vores kommunikations evner, empati og shared decision making med patienten, for at vide hvem de er, og hvad der er særligt vigtigt for dem, og om dette med rimelig sandsynlighed er opnåeligt (Ragland et al og Atul Gawande). Mine råd på området er derfor:
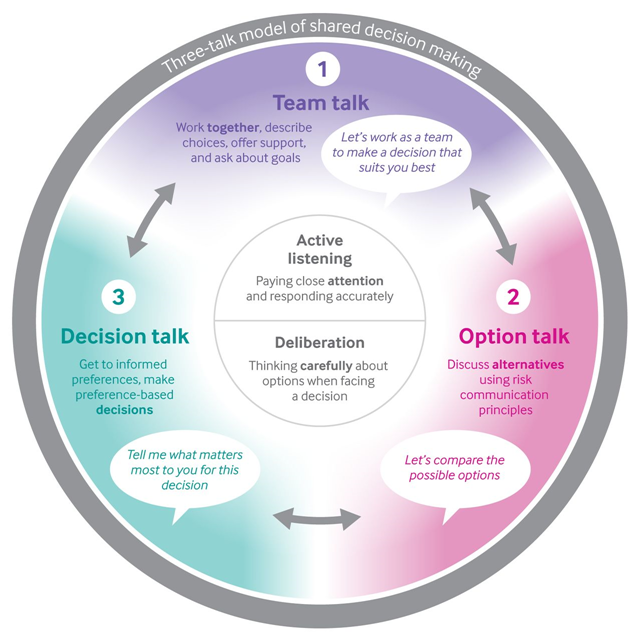
- Anvend kommunikationsevner til at skabe en relation og alliance: valider emotioner, anvend stilhed, aktiv lytning, husk navne m.m.m
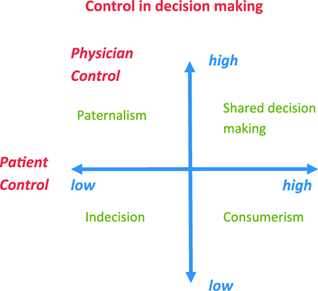
- Undgå at blive en statistik-maskine (atul gawande, Being mortal): ”informations-sælger” (consumerism) modellen, hvor man blot informerer om hvilke muligheder der findes, gør sig ikke så godt (men kan evt anvendes som en del af samtalen jf three talk modellen). Shared decision making er bedst som ekspert-modellen, hvor du som læge (ekspert i medicin), forsøger at møde patienten (ekspert i egen sygdom), og som et møde mellem to eksperter, udveksle jeres viden og præferencer. Således kan I komme frem til den bedste beslutning sammen:
- Har de lyst til at have samtalen lige nu? (hvis ikke, og deres tilstand er kritisk, informer dem på en ikke-truende måde om, at det kan være denne beslutning bliver taget for dem, skulle de få hjertestop)
- Hvor meget information ønsker det? (retten til ikke at vide)
- Hvad er deres forståelse af sygdomsprognosen? (som Atul Gawande skriver: “how we seek to spend our time may depend on how much time we perceive ourselves to have”)
- Hvad giver kvalitet for dem i livet, og hvor sandsynligt er det, at de kan få dette ved behandling (fx HLR)?
- Vær realistisk overfor dig selv, og patienten/pårørende:
- OHCA 1/10 overlever (formentlig lignende eller lidt mindre ved IHCA). Dog afhængigt af detaljer om- og timing til HLR – maximalt 30% ved OHCA med stødbar rytme. Betydeligt lavere med ikke-stødbar rytme.
- Godt neurologisk outcome? Et optimistisk skøn er ca halvdelen med ROSC har godt neurologisk outcome.
- Er man frail, er sandsynligheden for at overleve HLR 5-6% og med godt neurologisk outcome måske så lav som 1% (Nickels et al)
- Gør det klart, at vi altid gør, hvad der er i patientens bedste.
- Plant et frø: Du behøver IKKE færdiggøre samtalen i akutmodtagelsen, men du kan opstarte tanken om, at den skal foregå. Dette bryder måske isen til, at samtalen kan udføres senere i forløbet
- Pårørende er patientens advokater – det er vigtigt at fortælle patienter /pårørende, at de IKKE træffer beslutningen, men vi behøver dem, for at kunne forstå, hvad der er/var vigtigt for patienten
- Uenighed blandt pårørende og/eller patienten er OK – vi behøver IKKE en konsensus lige nu. Men skulle det pludseligt blive hjertestop, bliver det en lægelig beslutning, som bliver taget for dem
HLR er bare første skridt
Behandlingsbegrænsning stopper ikke ved HLR, og næste skridt er intensiv terapi (Intubation, dialyse, vasopresser behandling, akutte operationer), derefter ”fuld behandling på stuen” (antibiotika, væske m.v), derefter ”kærlig pleje” (smertelindrende, angstdæmpende m.v)
Patienten behøver ikke beslutte det hele fra start.
Held og lykke – du gør patienterne og hele forløbet en tjeneste:
“A few conclusions become clear when we understand this: that our most cruel failure in how we treat the sick and the aged is the failure to recognize that they have priorities beyond merely being safe and living longer; that the chance to shape one’s story is essential to sustaining meaning in life; that we have the opportunity to refashion our institutions, our culture, and our conversations in ways that transform the possibilities for the last chapters of everyone’s lives.”
Fra Being Mortal af Dr Atul Gawande
So, I think it will be much easier [to talk about dying]. For
Uddrag fra samtale med enkemand. Mandens kone døde af terminal cancer, og de havde en EOL samtale før dette skete. Fra Hanson et al, 2019: What matters at the end of life
me it has become easier, because it was a positive
experience, when we [his wife and him] discussed it [wishes at End Of Life] before she died. When I have to go away, I will use that again.
Take home
- EOL (end of life) og behandlingsbegrænsning bør være en standard del af enhver samtale med patienter i akutmodtagelsen – særligt fraile med multiple indlæggelser og faldende funktion, men i virkeligheden er det et generelt ønske, der stiger i prævalens med alder og dalende funktionsniveau
- Alle ældre har tænkt over EOL, og ved indlæggelse ønsker de fleste at tale om det med den rette person og i den rette situation. Særligt HLR ønsker man at tale om på akutmodtagelsen (mange forventer det)
- Plant et frø (samtalen behøver ikke afsluttes i akutmodtagelsen – men bare det at bringe emnet op, kan bryde isen for senere samtale under indlæggelsen)
- Vær realistisk – kun 1/10 overlever OHCA og formentlig lignende eller værre prognose med IHCA (men timingen til kompressioner, og overlevelse til 30% ved OHCA under optimale omstændigheder findes).
- Overlevelse er IKKE lig god neurologisk outcome. 1,1% af frail ældre har godt neurologisk outcome
- Pårørende er advokater for patienten og IKKE den, der tager den endelige beslutning – men vi behøver dem til at træffe vores fælles beslutning, da de har indsigt i hvad der er vigtigt for patienten

Kilder og inspiration til videre læsning
- DBI, St emlyns: http://www.stemlynsblog.org/jc-devastating-brain-injury-complex-decisions-in-the-resus-room-st-emlyns/
- Dansk hjertestop register, 2001-2016: http://genoplivning.dk/wp-content/uploads/2018/04/Dansk_Hjertestopregister2016.pdf
- Elwyn et al, 2017: three-talk model for shared decision making: multistage consultation process
- ERC 2015, section 5 – Nolan et al: Guidelines for post-resuscitation https://ercguidelines.elsevierresource.com/
- Estraneo, 2013: Predictors of recovery of responsiveness in prolonged anoxic vegetative state
- Gawande, Atul: Being mortal (bog)
- Stine Hanson, Mikkel Brabrand, Anne-marie Lassen, Jesper Ryg og Dorthe Nielsen, 2019: What matters at the end of life
- Harvey et al, 2018: Management of perceived devastating brain injury after hospital admission: a consensus statement from stakeholder professional organizations
- Laarhoven et al 2014: To Treat Or Not To Treat – who should decide?
- Nickels og Conroy et al, 2018: Geriatric emergency medicine
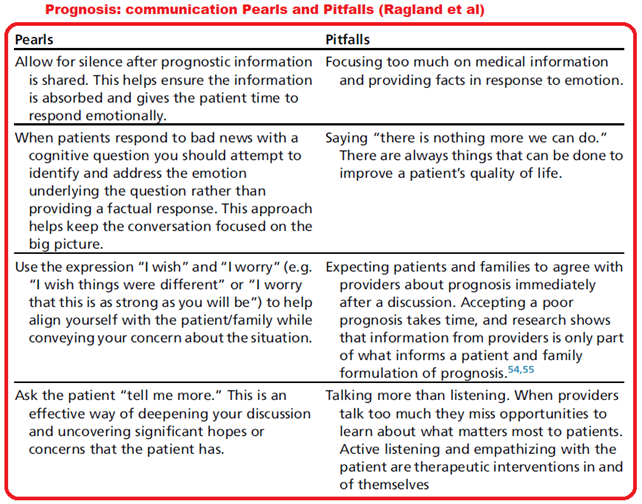
- Ragland et al: Adressing Prognosis in Serious Illness, 2017
- Sandroni et al, 2013: Prognostication in comatose survivors of cardiac arrest: An advisorystatement from the European Resuscitation Council and the EuropeanSociety of Intensive Care Medicine
- Sandroni et al 2018: Prognostication after cardiac arrest
- Sulzgruber et al, 2017: Age-specific prognostication after out-of-hospital cardiac arrest – The ethical dilemma between ‘life-sustaining treatment’ and ‘the right to die’ in the elderly.

