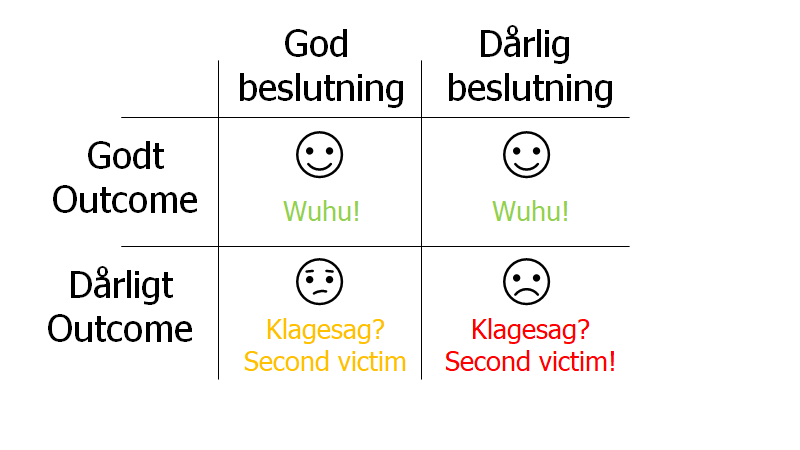
Den usynlige patientrisiko er noget som ikke fremgår af statistikken, og noget vi sjældent forklarer om til patienterne. Det er noget, som dræber mange patienter årligt, og skaber angst og nedsat livskvalitet dagligt for vores patienter, samt ikke mindst crowding og access block.
Det er noget, der rører ved vores inderste eksistentielle angst for både patienten og lægen.
Overdiagnostik gennemsyrer vores sundhedssystem, og dets løsning er kompleks. Det er ikke bare behandling og diagnostik, men også henvisning til for højt niveau i sundhedssystemet for tidligt i forløbet. Det er drevet af flere ting, og jeg nævner kun nogle her i denne blog:
- Toksisk fejlkultur (se også del 1: safe container) og manglende rum til at tale om angst og sårbarhed som læger, og risk proximity begrebet.
- Manglende tid (manglende evne til at tage os tid) til at kommunikere og skabe alliance med patienten, og udføre shared decision making, når vejen ikke er helt klarlagt
- Tiltagende politiker / befolkningsønske om at alt løses på samme dag, og dermed underminering af en af vores bedste tests: Time as a test / regression to the mean
- At vi ikke har en grænse for, hvornår noget er “udelukket” (acceptable miss rate)
- Tendens til snæversynethed i vores kvalitetsmål: vi måles på tid – men tiden stopper ikke, når patienten går fra akutmodtagelsen. Vi har incitement til at smide patienten videre hurtigt, i stedet for at levere kvalitet
Samtidig med alt dette, skal vi også tænke på, hvad risiko er – og at fortolkningen af risiko varierer med personlighed, erfaring, alder, demografi m.m . Alex Honold har fx internaliseret så stor en del af sin højdeskræk, og ville aldrig gøre det han gør, hvis han ikke mente det var relativt sikkert. Derimod mener han, at risiko for ham i større grad fx er det vi alle gør – at spise usundt og ikke motionere
OK – Here we go:
Det usynlige patientusikre system
Den usynlige patientusikkerhed i systemet bliver måske tydeligere og tydeligere igennem mine blogs: Overdiagnosticeringen!
Tidlige besøg
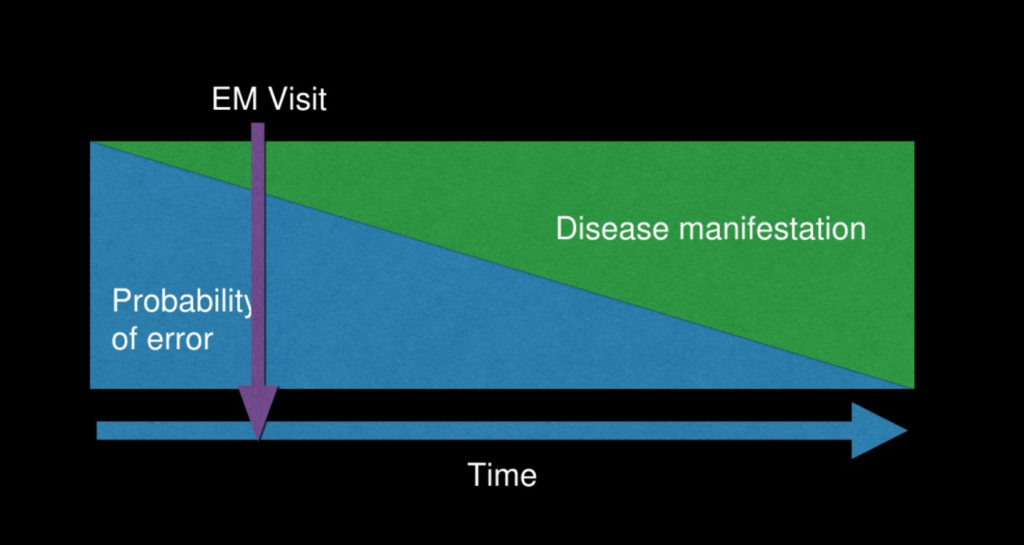
Det der sjældent forstås er, at når man ser på det prospektivt (fx 21 årig kvinde med feber uden andre symptomer, der endte med at have meningit), så er det svært at 1: se, at mange kollegaer med de oplysninger man havde, ville have gjort anderledes (er det så en “fejl”?), 2: såfremt man skulle ændre noget ud fra den læring man nu har fået – hvilken regel vil man så applicere på den 21 årige feber patient . Ville blodprøver have ændret noget? Nej – men skal skal alle så lumbalpunkteres? Hvilke konsekvenser har det for alle andre patienter, der må vente?
Patienter forsvinder ikke, når de går fra vores afdeling. De må informeres og er vi virkelig urolige, må vi sikre os, at de har nogen, der kan reagere på deres vegne. Kommuniker tankerne til dem: Kommer en patient tidligt i forløbet, må vi være pragmatiske og fortælle, at alt ikke kan gøres nu, hvis man bedømmer dem lav-risiko, og bede dem komme tilbage. Selvom retrospektoskopet er angstprovokerende, så indtil vi opfinder tidsmaskiner, så lever vi altså fortsat prospektivt.
Vil man investere i noget, så er det måske klinisk feedback og oplæring i kritisk tankegang og kommunikation, samt ændre de mere komplekse problemer i systemet (se del 2)
Case: 30 årig mor, møder med sin kæreste på natten, da hun har haft et “stirrende blik” og været svær at tale med i nogle få sekunder synes kæresten. Flere er syge hjemme, og hun har haft feber i 3 dage, ikke drukket / spist så meget og ligget på sofaen. Opkastninger, uden diaré og muskelsmerter er hendes øvrige klager. Ved ankomst har hun vitalparametre: SAT 100%, BT 130/90, puls 110, Tp 39,6 (øret). Efter panodil (som hun ikke har prøvet tidligere) har hun Puls 90, Tp 37,5 og er lidt træt, men ellers helt upåvirket når du ser hende. Ingen misbrug, hoster en enkelt gang ved undersøgelsen, ej nakkerygstiv. Du er ved at sende hende hjem, da du ser, at man i triagen har taget blodprøver, med CRP 230, LKC 8, K+ 3,1 – ellers normale prøver. Du ser patienten på en svensk akutmodtagelse, og patienten er derfor kommet ind uden visitation via en anden læge
Når en patient står foran en læge, så er er meget gået forud for dette besøg. Vi ved, at sygdomme (og sygdomsfølelse = illness) har et spontantforløb, og hvornår patienten præsenterer i sygdomsforløbet er noget vi ikke altid tænker på, men som har monumental vigtighed.
Der findes for de fleste patienter en hvis tærskel for at gå til læge. Derfor vil de færreste gå til læge ved mindre hverdagssymptomer.
Denne barriere for at gå til læge fungerer dermed som et (mener jeg) nødvendigt filter, og når vi tager dette filter væk (fx introducerer telefonvisitation, eller åbne akutmodtagelser), vil vi pludseligt se, at patienter søger tidligere i deres sygdomsforløb (selveste Scott Weingart mener, at dette er en af de største problemer i akutmedicin i dag)
Dette er ikke noget problem, hvis patienten er villig til at få at vide “du er kommet for tidligt til, kom igen, hvis det bliver værrere” (dvs vigtigheden af follow-up og eget ansvar hos patienten – dette nævnes som en af de vigtigste løsninger i EmCases Ep 129 om crowding). Patienter vil dog helst have alting fixet på én gang i dag (tænk selv over det – vil du ikke også det i banken? når du bestiller mad? når du booker rejser?). Det er den standard og det samfund, vi er blevet vant til i dag.
Dette volder dog (efter min mening) et enormt problem for patientsikkerheden (Ja! patientsikkerheden! – det er paradoxalt kære politikere, men følg nu med):
Ofte vil patienten tidligt i sit sygdomsforløb nemlig være under en test-tærskel- og en behandlngstærskel. Men behovet for at få “fixet” alting på én gang gør, at folk ikke vil “gå forgæves” (selvom det ikke er tilfældet – de får en lægevurdering), og ofte vil spørge om de ikke skal fx have en blodprøve eller have en antibiotika kur just in case. En effekt af, at folk kommer tidligere i sygdomsforløbet, gør logiskt også, at flere patienter kommer til lægen (simpelthen fordi majoriteten med sygdomsfølelse vil gå over med nogle dages venten). Ikke alene har lægen derfor færre minutter pr patient, men også kortere tid til at kommunikere, hvorfor patienten ikke skal have en test / behandling. Som vi kan se herover, så kan det være svært at forklare på kort tid – som min far i almen praksis ofte har sagt for at advare: det tager 10 minutter at forklare patienten hvorfor de ikke skal have antibiotika. Det tager 2 minutter at udskrive det
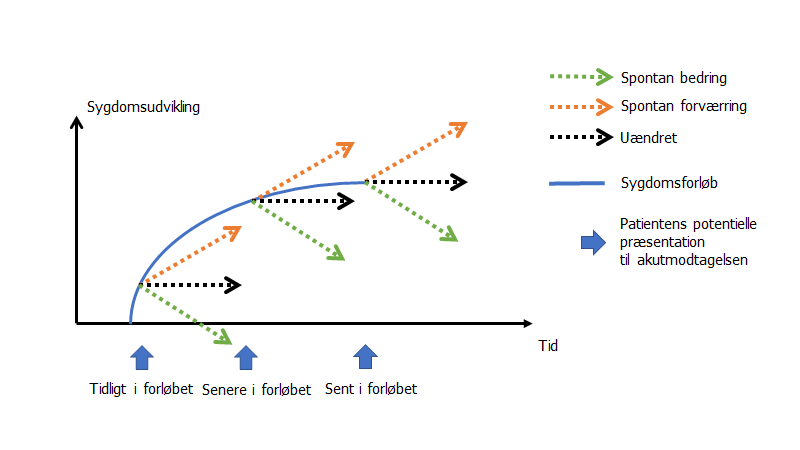
Inden jeg går videre, vil jeg lige bemærke nogle ting ved overstående grafiske fremstilling af sygdomsforløbet
- Tid: jeg har bevidst ikke sat “dage” eller “timer” på. Tiden for hvor hurtigt et sygdomsforløb udvikler sig er helt afhængigt af tilstanden. Et stroke udvikler sig over sekunder, og “peak”-sygdomsudvikling er ofte efter få timer, hvor der ikke længere er tvivl om diagnosen
- Sort- og rød pil: spontan forværring af sygdomsfølelse betyder ikke, at patienten tager skade (og det nævner jeg ofte for dem). Har patienten en psykosomatisk årsag som ikke er addresseret, vil patientens lidelse fortsætte og udvikles, trods det ikke repræsenterer en farlig tilstand (fravær af bedring og forværring er altså ikke nødvendigvist et dårligt tegn, hvis tidskritiske årsag er bedømt ude). Dette nævner jeg til mine patienter ved afslutningssamtalen (gå til læge hvis det ikke er blevet bedre om xx dage – det betyder ikke nødvendigvist at tilstanden er alvorlig, men at hvis du har invaliderende symptomer, skal fortsætte med at kigge på det)
Summa sumarum: frit valg på alle hylder er ikke bedre for patienten – spørg enhver læge. Ved at gøre lægebesøg og tests mere tilgængelige for befolkningen, mister vi som læger en af de bedste tests – patientens egen følelse af sygdom der får dem til at søge læge. Det filter forhindrer ofte overdiagnostik (for detaljer, se bloggen “erfaringer fra Sverige”)
Tid som (den vigtigste) test
Jeg håber det er klart ud fra overstående, at vi altså ikke kan (eller skal) undersøge eller behandle patienten, hvis de kommer for tidligt i forløbet. Dette ser vi ofte ved, at patienten efter vores bedømmelse er under en test tærskel / behandlings tærskel.
Et andet relateret koncept er, at post-test sandsynligheden kun kan komme så langt ned på ét besøg. Studier på fx Lungeemboli og AKS har vist, at yderligere undersøgelser ofte fører større problemer med sig i form af downstream undersøgelser af falskpositive resultater og komplikationer og angst hos patienten (til dels pga manglende addressering af hvorfor de rent faktisk kom til lægen – “du får en test, og er det negativt er det OK”, kan ikke erstatte kommunikaton)
Sygdomsforløb vil ofte gå i sig selv igen, og årsagen til at du er dårlig, er pga daglige flukturationer. Disse variationer sker omkring en baseline (mean), som du vil falde tilbage til:
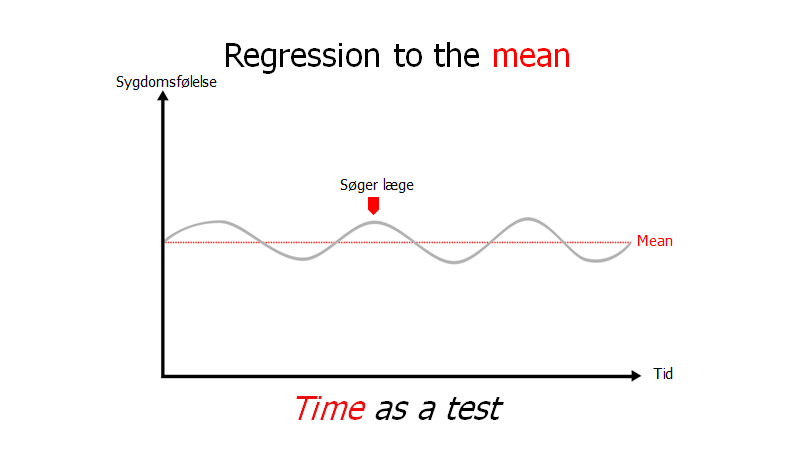
Patenten søger ofte læge når de er allersygest ift deres base-line. Er de lav-risiko for tidskritisk sygdom på akutmodtagelsen, efter relevant udredning, er det oftest bedre at slippe dem og lade tiden være en test.
Denne kurve kan fx også anvendes til at forklare hvorfor patienten med højt blodtryk på akutmodtagelsen bliver nødt til at få målt det i stabil fase, før man kan sige noget sikkert, og ved, hvad man behandler på
Ud fra regression to the mean er det logisk, at tiden er en test, og der er i et velfungerende sundhedssystem nødt til at være plads og follow-up mulighed til at vi kan anvende denne vigtige test!
Har patienten kroniske problemer kan det ud fra samme model være pga baseline ændring (mean ændring):
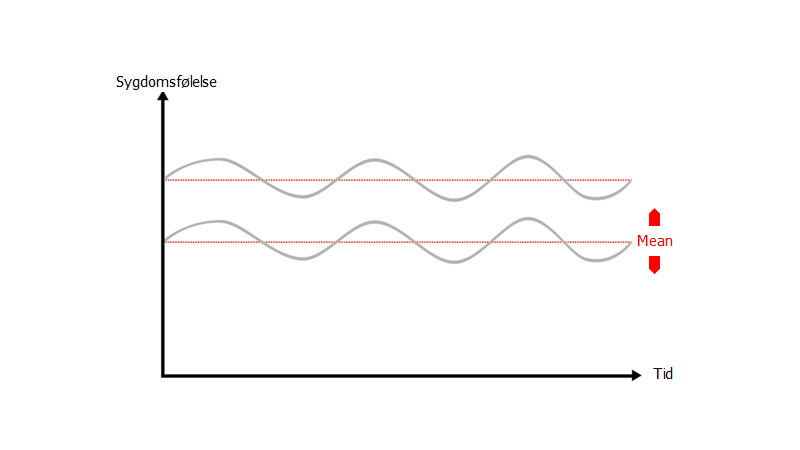
Vi fortæller ofte patienterne, at de skal søge egen læge, hvis det ikke bliver bedre. Det er hér vigtigt at fostå følgende:
Patientens sygdom kan afhænge af enten
a) fluktuation omkring deres baseline jf grå linje og figuren herover (regression to the mean) (mere akut fra dag til dag)
ELLER
b) Ændring af deres baseline (mere kronisk – over måneder. Obs: de svarer ofte “nej” til spørgsmålet om de er stressede. En del af årsagen kan ofte være, at de er nødt til at dissociere sig fra stressen, indtil den kommer ud som somatisk symptom)
Patientens baseline afhænger af ressourcer og stressorer ( (fx homeostatisk ubalance – spiser, sover, drikker, motionerer, socialiserer ikke optimalt over længere tid ; uhensigtsmæssig coping: pain avoidance etc). Man kan fx spørge en patient man er i tvivl om, har en dårlig baseline eller blot fluktuation: “hvornår var du sidst rigtig dig selv / rigtig rask?” (svarer de lang tid siden, er det oftere med kronisk årsag)
Når man har dårlig baseline, skal der forholdsvist mindre til at søge læge (man føler sig sygere) – flutkuationerne (grå linje) komer indenfor rammen af sygdomsfølelse oftere. Selvom tilstandens årsag ikke er mere livstruende, så føles den meget stærkere. Det er ekstremt vigtigt, at vi er opmærksomme på “lidelsen” for disse patienter også, og at det de behøver er ikke at somatiseres (fx stil ikke pseudodiagnoser, bestil ikke unødige prøver). Hjælp dem med at forstå, hvad der sker og tal i sandsynligheder ift bio-psyko-social modellen (“det der sker for dig, er mindre og mindre sandsynligt biologisk. Det er vigtigt, at vi kigger på mentale og sociale årsager også!” – husk validering og normalisering!: “det er normalt, og er ikke noget man gør bevidst. Men tager vi ikke også fat i disse del-komponenter, bliver det ikke bedre”)
Det er desuden vigtigt at fostå, at patienten IKKE kan skelne UDEN din hjælp som læge. Ekstreme symptomer kan ligesåvel være rent base-line problemer, med evt mild somatisk komponent (majoriteten af de patienter jeg ser i akutmodtagelsen i Sverige). Der skal skelnes mellem
a) Skade på kroppen (biologisk komponent)
b) Lidelse (patientens følelse ud fra mentale, og sociale faktorer – ressourcer Vs stressorer)
For detaljer, vent på kommende blog om somatisering og funktionelle tilstande
For simple råd til patienten: “understanding pain in 5 min or less (youtube)”; DrMikeEvans: Having a crap week (back to basics)
Patientens empowerment og shared decision making: er patienten lavet af glas?
Overstående har altid været sandt for lægegerningen, og den usikkerhed det medfører er noget vi – før vi får perfekte test der ikke vil overdiagnosticere ved at udføre dem på et hvert tidspunkt i sygdomsforløbet – altså må blive vant til. Også selvom politiske unuancerede holdninger vil, at vi kan alt på ét besøg. Som jeg tidligere har pointeret, så er vi ikke en McDonalds (som almen praksis, som akutmodtagelse, som ambulatorie eller som afdeling).
Det betyder, at vi unægteligt sender nogle patienter hjem, som vil blive værre (SELVFØLGELIG også fra akutmodtagelserne).
Lad os kigge på akutmodtagelsen, og den population vi sender hjem derfra. Man kan se fordelingen af outcomes ud fra denne karikerede model:
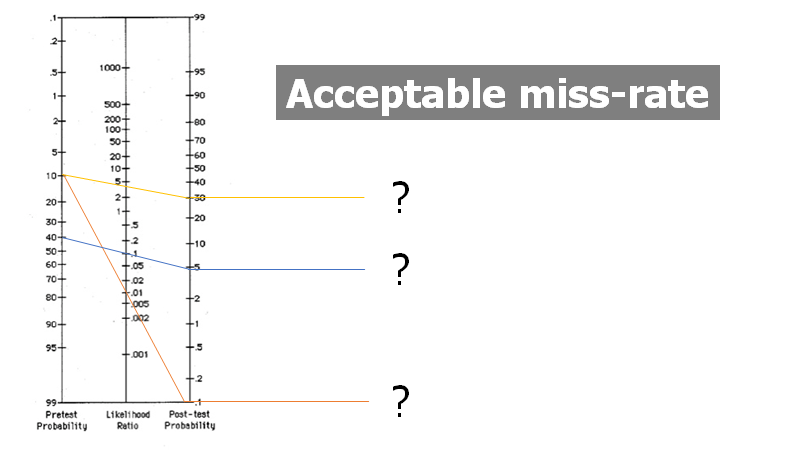
Har jeg i casen sænket sandsynligeheden langt nok? Hvordan kunne den yderligere sænkes?
Bemærk i figuren herunder – proportionerne af patienter, der “misses” bliver større, jo større post-test sandsynlighed du sender dem hjem med. Det betyder dog ikke, at patienter der “får konsekvenser af en missed diagnose” bliver større (de fleste tilstande kræver ingen diagnose – og at “misse” dem, er kun vigtigt at undgå, hvis de er farlige eller alvorlig invaliderende)
Vil vores patient i casen kunne komme tilbage, hvis hun skulle blive dårligere? Hvor sandsynligt er det, at tilstanden, hvor vi står i sygdomsforløbet lige nu, er så alvorlig, at dette er umuligt og forværringen fra der hvor hun står nu, vil dræbe hende?
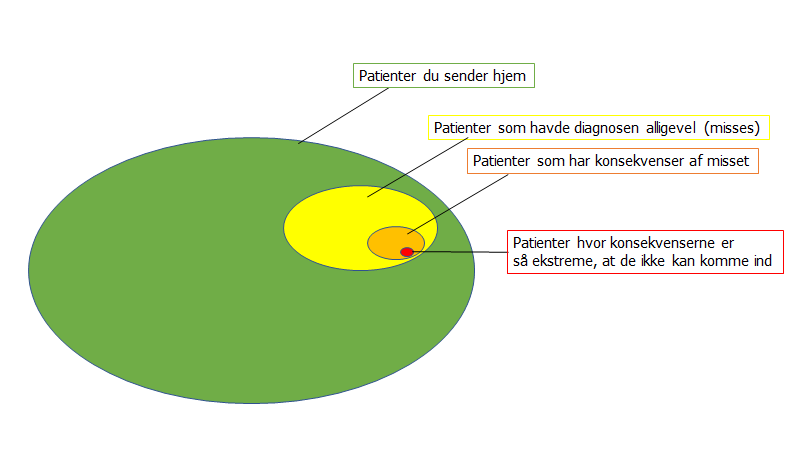
De forsvinder ikke ned i et sort hul, når de forlader akutmodtagelsen – ofte når vi laver en suboptimal udredning, er vi heldige og der sker ikke noget med patienten (grøn). Sjældent havde de faktisk diagnosen (gul) og får konsekvenser af diagnosen (orange). Endnu sjældnere, er disse konsekvenser så alvorlige, at de aldrig får mulighed for at komme ind igen (rød)
Ofte må vi købe tid (alt kan og skal ikke udredes når du ser patienten i øjeblikket) – fordi tiden er en test – før patienten enten spontant bliver bedre (regression to the mean) eller forværres i en grad så de kommer over test-threshold. Jf også figurerne herunder “time as a test” og “regression to the mean”
Et eksempel på overstående koncepter, er patienter der kommer hurtigt ind med mavesmerter og efter relevant klinisk udredning, har lav post-test sandsynlighed for appendicit. Der er ingen yderligere test, andet end operation, der kan afgøre noget i dette øjeblik du står i nu. Derfor er det bedre at sende dem hjem (da mange viser sig ikke at være noget, og de, der viser sig at være noget, kan komme tilbage dagen efter til kontrol)
Hvis du selv vil prøve med en rigtig udfordring, så tænk over hele borrelia og neuroborrelia spørgsmålet (en blog der er på vej snart) – Patienten med vage symptomer (fx monosymptomatisk hovedpine og træthed) og en positiv borrelia blodprøve IgM. Hvornår giver det nogensinde mening med blodprøver? Er det farligt at lade være at behandle en borrelia? Hvor mange skal behandles før du forhindrer en farlig neuroborrelia? Hvor mange med neuroborrelia går i sig selv igen?
Caseafslutning: Da patienten er kommet fra gaden i Sverige, tilhører hun en low-acuity population. Ifølge bayes teori, når hun tilhører en lav-risiko gruppe, skal hun have en meget farlig historie for at rule in for videre tests eller behandlinger. Ud fra din kliniske bedømning, er du ikke bekymret for patienten, og du ville ikke have taget blodprøver på patienten, havde du selv set hende i triagen – altså er hun under en test-tærskel, og testen skal derfor fortolkes med en lav præ-test sandsynlighed (lav risiko population, atypisk historie, almen tilstand upåvirket, intet oplagt fokus). Der er intet umiddelbart fokus kliniskt, og selvom du har oplysningerne nu med CRP >200 (LR+5 for pneumoni), kan du ikke se, hvordan flere tests vil ændre din behandling (vil et røntgen af lungerne skelne mellem viral eller bakteriel? Vil dyrkning skelne?). Du udfører shared decision making med patienten, og anbefaler, at hun kommer tilbage om to til tre dage, hvis det ikke er blevet bedre til nye blodprøver. I mellemtiden anbefales panodil og fokus på væske.
Patienten kom tilbage få dage efter med en CRP uændret på 230, og man valgte at udføre et røntgen af thorax der viste basalt unilateralt infiltrat. Man valgte at opstarte antibiotika for mistanke om bakteriel pneumoni.
Hvad vil du bedømme post-test sandsynligheden for at dette er sandt, er? er post-test sandsynligheden (uanset diagnose) over en behandlingstærskel, som foreslås i casen?
Bemærk ved casen følgende take-home points
- Det er ikke en fejl at sende patienter hjem, der kommer tilbage, hvis der findes et godt resonoment og gerne en SDM (shared decision making) omkring det (gode beslutninger kan have “dårligt” outcome)
- Tests kan ikke fortolkes uden præ-test sandsynlighed (undgå “ready, fire…aim” (Schecter et al, 1985) = Vi behandler patienten – ikke blodprøven. Se på hvordan patienten ser ud, og dan dit eget indtryk (gestalt) før du kigger på blodprøverne.
- “Time as a test”, er essentielt at kende til som modtagende læge for at undgå overbehandling- og overdiagnostik
- Hvis håndteringen af patientens problem ikke ændrer ud fra en diagnotisk tests resultat, så undlad at bestille den (fx røntgen af thorax)
- Tænk altid på hvilken population patienten tilhører – kommer patienten fra gaden, er de en primær-sektor population, og er generelt lav-risiko (medmindre din patient tilhører en særlig høj-risiko mikro-population fx turister feber eller misbrugere med feber)
Take home er hér: den “usynlige” patient-usikkerhed (i form af overdiagnostik, manglende tid til faktisk kommunikation og crowding), der skabes ved at bestille (unødige) tests og behandlinger når patienten er under en test tærskel og/eller kommer tidligt i forløbet, skal bekæmpes. En af måderne er time as a test konceptet, og test thresholds. Det nytter ingenting, at systemet kæmper imod os, og hvis der efter politikere, patienter og andre interessehavere fortsat er uenighed efter de har forstået overstående, så må vi komme til en fælles løsning som besluttes af alle parter involveret jf Jeffrey Braithwaite 2018: Changing how we think about improvements.

Simon Carley plejer at sige: Vi er ikke diagnostikere – vi er probabilistikere i akutmedicin særligt, men generelt som læger.
Sproget er nødt til at ændre sig med vores patienter, blandt kollegaer og i systemet som helhed. Dette er en af mine kæpheste, da det er så vigtigt for hele sundhedssystemet og er en stor del af årsag til lidelse for læger og patienter
Lad mig forklare hvorfor
Pas på “falske dikotomier”: Ifølge probabilistisk tankegang (Bayes) er ting altid på et spektrum af sandsynlighed (jf fagans nomogram, præ-test- og post-test sandsynlighed). Men i vores sprog med vores kollegaer og med vores patienter er dette ikke illustreret. Dette er en simpel, men ekstremt vigtig og paradigmeændrende tilgang til klinisk sprog:
Ord der bør rafineres / udgå eller ”probabilisticeres”:
– Fejl” og “Fejldiagnostik”: Disse koncepter er eksisterer ikke i den udstrækning som vi tror det gør, men er grove simplificeringer: When you do miss the one patient. Well, you don’t miss them, it’s just an inevitability that you go through these (diagnostics) processes, that patient don’t get diagnosed. They are not missed, they just don’t get diagnosed. Det betyder ikke, at vi ikke kan lære når der er UTH’er i systemet. Det betyder bare at ansvaret placeret ved en enkelt person (lægen) er en grov forsimpling, og tyder i de fleste tilfælde på manglende forståelse af probabilisme og systemets komplexitet (se Braithwaite 2018). Second victim syndrome, og åben, tilgivende og støttende ”fejl”-kultur: En konsekvens af overstående er, at vi alle vil komme ud for at ”misse” en patients alvorlige tilstand på et tidspunkt i karriere (det er rent statistik). Se Second Victim Syndrome, og overvej hvordan lov-systemet kan tage højde for, så vi ikke går i Risk Proximity og overdiagnostik problemet: “It’s a good thing to be at the point where you miss something, because pursuing something to the absolute N’th degree, you start to create problems”
“
Diagnose (særligt i akutmodtagelsen, bør dette ord sjældent forekommer): Patienter har ikke diagnoser – de har sandsynligheder for diagnose (vi har et ord for det: tentative diagnoser!). Hvorfor kan vi ikke gradere tentative diagnoser. Put sandsynligheder på med fx ekstrem lav, lav, moderat, høj, meget høj risiko – så den næste læge ved, hvad du har tænkt. Jeg ved, at sundhedsstyrelsen ønsker, at vi diagnosticerer patienter. Men forstår sundhedsstyrelsen begreberne vi taler om hér? Og den fare det medbringer, at sætte diagnoser på noget, som er med lav sikkerhed bare fordi patienten skal udskrives med en diagnose, der ikke er en ”symptom-diagnose”. Et modargument kan være patienten diagnosticeret med UVI x flere. Når vi siger ”UVI” x flere – hvad menes så? Hvordan blev det diagnosticeret? D+R, klassiske symptomer? Gestalt? Vær altid skeptisk overfor diagnoser, hvis du ikke selv har læst hvordan de er blevet diagnosticerede (EmCases Ep 94: UTI myths and misconceptions – Suzanne O’sullivan skriver s. 68 om problemet med “journal-spøgelsesdiagnoser”: “At the top of each letter was a list of medical problems. The most recent one read: migraine, arthritis, angina, IBS, possible hypertension, abnormal liver function tests […]. I recognized the list, I had seen many like it before. It was the list that one junior doctor copies from the most recent letter in the notes into the letter they are currently writing. Lack of experience sees them underestimate the necessity of checking every fact. In that way a medical history can take the form of Chinese Whispers. “Chest pain under investigation” is slowly transformed into “angina” […]. A readthrough of her notes told me it had been ruled out, even though the diagnosis lived on in the legend of her letter”. Vi kender alle til dette problem. Det bliver ikke løst af overstående – men sættes tentative diagnoser på, VED VI, at vi skal kigge efter i journalerne efter hvad undersøgelserne faktisk viste. Det gør vi ikke, hvis det er en ”diagnose” (= sat i sten, kan aldrig ændres)
– Pas på sproglige ”premature closures” og inducering af ”diagnostic momentum” med dine ord: Kald det fx ikke ”afasi”, men ”sprogforstyrrelse bedømt som afasi fordi xx og yy”, og kald det ikke ”synkope”, men ”anfald / overgående bevidsthedstab / TLOC” – synkope ”framer” dig til at tænke på ikke-neurologiske årsager
– Afslutningssamtalen: Patienten har ALTID en post-test sandsynlighed. Vi må acceptere en ”acceptabel miss rate” alt efter farligheden af sygdommen, effekten / bivirkningerne af behandlingen mod sygdommen og vores test evne til at opfange den, samt patient-relaterede ønsker / værdier. Denne post-test sandsynlighed skal
”udelukket”: findes ikke i probabilistisk tankegang. Det nærmeste du kommer er ”ekstrem usandsynligt”. Begrund gerne din statement (fordi xx, yy og zz)
Regression to the mean og “time is a test” er vigtige diagnostiske koncepter, som vi kunne anvende mere, hvis vi anvendte probabilistisk sprog som diagnostiske værktøjer
Nogle vil måske argumentere, at nogle patienter behøver ”dikotomt” sprog (“alt er udelukket”) – men vi skal ikke beskytte patienterne imod sig selv. Den ”eksistentielle angst”, kan vi (som Bent Falk beskriver) aldrig tage fra patienten.
Som Cervellin et al, 2014 beskriver: “There is no single test that is able to definitely identify a
‘‘healthy status’’, so that emotional requests from patients who seek reassurance of being ‘‘healthy’’ with a large battery of diagnostic tests should not be honored”
Omvendt tror jeg den “disney-historie” vi ofte forsøger at fortælle patienterne (“alt er udelukket”) i sidste ende er paternalistisk, og fratager dem eget ansvar for sundhed.


Alle tests har falsk positive, og falsk negative, ligeså vel som (sandt) negative og (sandt) positive. Hvert scenarie giver anledning til behandling, der enten kan a) gavne (hvis sandt positiv eller sandt negativ), b) ikke ændre noget, eller c) skade
Greenberg 2014: Over-testing: Why More Is Not Better skriver:
There are at least 5 reasons why clinicians over-test:
1) Belief that ordering many tests will help detect subclinical
disease
2) Defensive medicine
3) Lack of knowledge or confidence
4) Patients’ expectations
5) Profit
When ordering unproven screening tests for asymptomatic patients without good reason, few consider the low yield, high cost per diagnosis made, and considerable toll of false positives. Anecdotal accounts of unexpected diagnoses discovered on “routine” testing help perpetuate over-testing. But even the best tests yield more false positives than true positives when the prevalence of what one is testing for is low. Others order tests to establish a “baseline,” but this has been shown repeatedly not to improve care for asymptomatic patients and consumes hundreds of millions of health care dollars per year. Abnormal results that later prove erroneous engender unnecessary anxiety and needless follow-up testing. Ordering only medically indicated tests reduces our role as instigators of needless worry and, as an added benefit, helps lessen physicians’ workload […]Abnormal results that later prove erroneous engender unnecessary anxiety and needless follow-up testing. Ordering only medically indicated tests reduces our role as instigators of needless worry and, as an added benefit, helps lessen physicians’ workload.
Rosenbaum 2017 The Less-Is-More Crusade – Are We Overmedicalizing or Oversimplifying? påminder os om balancen
“the most accurate conclusion is that sometimes less is more, sometimes more is more, and often we just don’t know “
Det er dog ikke fordi vi er dovne, at vi ikke vil teste mere, men fordi det SKADER PATIENTEN, og vi spenderer tid på test som dårlig erstatning for kommunikation og tolerering af usikkerhed:
“When a test isn’t necessary, time can be more appropriately spent counseling patients, listening to them, and redoubling efforts to follow well-supported preventive guidelines” (Greenberg)
Denne tid kunne altså spenderes på at forklare overstående figur lidt bedre til patienten, så de ikke er hunderæd og unødigt lider, når vi ligger dem ind. I Newman et al, 2015: Quantifying Patient-Physician Communication and Perceptions of Risk During Admissions for Possible Acute Coronary Syndrome, tydeliggøres dette i diskrepansen imellem lægens mistanke om alvorlig sygdom og motivation for indlæggelse (i dette tilfælde lav-risiko chest pain) VS patientens egen forståelse
“A discussion regarding the possible risks to patients and reasons for remaining in the hospital only occurred 2/3 of the time. Patients and their physicians only agreed on the patient’s risk 36% of the time. Additionally, patient estimation of MI mortality at home versus in the hospital was 80% v 10%; while physician estimation was 15% and 10%”
Billedekilde: Egen model af model fra St emlyns – Risky Business part 5

Vi skal desuden huske, at patienten ofte ønsker vores VURDERING – de kan ikke bruge medicin eller diagnostiske undersøgelser til noget, andet end at gøre dem raske og/eller finde ud af, hvad der er galt med dem. Kommunikaton og forventningsafstemning er hér essentielle.
Og ofte vil en afvisning af patientens ønske IKKE føre til nedsat patient-tilfredshed (tværtimod). Uanset skal vi huske på, at patienttilfredshed IKKE er vores primære mål af overstående illustrerede grunde (vi har en samfunds-lægelig opgave også ved fx antibiotika, CT skanningsressourcer etc)
Justin Morgenstern fra First10Em beskriver dette fint: ” Ultimately, I think this number [jf blogindlægget Paying patients to forgo head CT (Iyengar 2019)] provides important insight into the limits of shared decision making. If the harms of a test clearly outweigh the benefits, it shouldn’t be offered. Patient satisfaction should not overrule good medical care. Our responsibility as doctors sometimes involves protecting patients from themselves. Shared decision making is a wonderful tool when there is truly equipoise. It should be used when the harms and benefits are evenly matched. It should be used when the harms and benefits are qualitatively different, requiring a judgement call in priorities. It should be used when there is significant uncertainty about the actual harms and benefits. However, it shouldn’t be used when one option is clearly better than another
EmCases Ep 49 beskriver
” Patient Centered Care is an approach to care that can be defined as care based on respect for patient’s values, preferences, and expressed needs. It involves building partnerships with the patient and family, and encouraging them to actively engage in their own care.
Patient Centered Care is not offering patients anything they want (i.e. antibiotics for a viral illness or narcotics). Wishes should be honored, but not mindlessly acted on.
Patient Satisfaction, on the other hand is defined by the patient’s experience; the perception the patient is left with after the health care encounter. This is a subjective concept, which is not necessarily associated with quality of care. While studies on patient centered care have generally shown improved outcomes, studies on patient satisfaction have been inconsistent. Some studies have shown that better patient satisfaction is associated with higher mortality rates and poorer patient outcomes
One must integrate the patient’s values and expectations with evidence-based medicine in order to provide excellent care.
Jf fx BroomeDocs: PODCAST: Shared decision making ; Emcases: Episode 49 Effective Patient Communication, Patient Centered Care and Patient Satisfaction, First10Em: Paying patients to forgo head CT (Iyengar 2019)
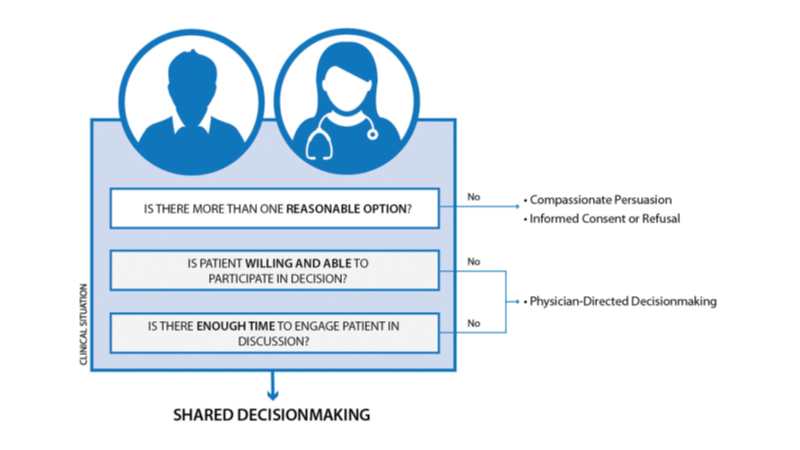
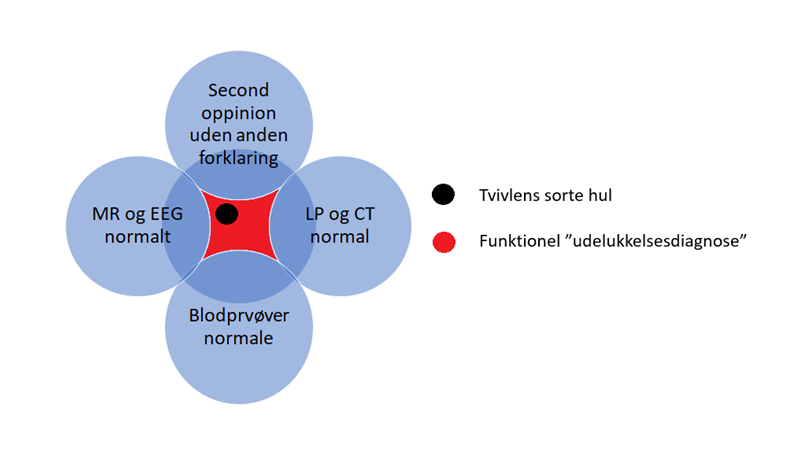
Den eksistentielle angst, vil vi aldrig være i stand til at fjerne fra patienten – uanset mængden af test. Både vi som læger, og patienten kan blive fanget i tvivlens sorte hul: Har vi nu udelukket alt? Er du sikker på, at du ved nok om det her, og har overvejet alt?
Hvornår grænsen sættes for “tilstrækkelig udredning”, er elastisk. Men den skal sættes på et tidspunkt. Når den er sat, betyder det ikke, at nye symptomer eller ændring i symptomer skal ignoreres – de skal tages ligeså seriøst (hvorfor det kan være en idé at have en oversigt over symptomer patienten har, hvis det er kroniske problemer med mange symptomer – en oversigt, så man ved, hvad der er nyt og gammelt)
Hullet lukkes med håndtering af usikkerhed, forståelse, gennemsigtighed, ydmyghed og ærlig kommunikation med patienten om probabilistisk viden om deres tilstand
Nogle meget sigende quotes om problemet, findes i Suzanne O’sullivans bog – it’s all in your head, 2016:
“there is a terribly delicate balance in the investigation of benign-sounding symptoms. One must investigate to rule out a physical cause if it seems necessary, but the line where investitagions should be stopped is drawn very faintly” (Suzanne O’sullivan, it’s all in your head)
”Blood tests, X-rays, every test comes with the same risk. Some tests are particularly difficult to interpret and therefore open to errors. To carry out a test is not a benign procedure, so I made a deal with D (patient)” (Suzanne O’sullivan, it’s all in your head)
“Where a diagnosis cannot be clearly demonstrated with positive tests, doubt has room to grow. Where the mechanism of a illness is poorly understood, questions flourish. To a person struggling against the possibility of a psychological diagnosis, the unknowns create a hiding place” (Suzanne O’sullivan, it’s all in your head)
“As it is the doctor’s job to allay the patient’s fears and dispel any confusion about the diagnosis, a problem arises if the doctor is not convinced” (Suzanne O’sullivan, it’s all in your head)
“he feels a pain in his back that he immediately suspects – no, he KNOWS – is something very serious […] One week later he sees his doctor again and is told that the X-ray is completely normal. ”But that is impossible!”, says D (patient). His GP sends him home and tells him to stop worrying. D (patient) does not stop worrying. He has not yet been given a satisfactory explanation for his pain and he wants to see another doctor and to have more tests” (Suzanne O’sullivan, it’s all in your head)
For detaljer: Jf bl.a Suzanne O’sullivan, It’s all in your head
Gode og dårlige outcomes er ikke det samme som gode og dårlige beslutninger
Mit råd er, når du “misser” en diagnose (en patient kommer tilbage med den sygdom som du har forsøgt at udelukke – fx en sinusvenetrombose), at spørge dine kollegaer prospektivt om casen (ikke retrospektivt), og spørge dig selv/dine kollegaer bagefter – hvis jeg skal lave en regel ud af denne oplevelse, hvad vil jeg så ændre til næste gang? Hvilke konsekvenser vil det have for populationen som patienten tilhørte (fx alle unge kvindlige patienter med progressiv hovedpine over 2 dage og lysfølsomhed), bliver groft overbehandlet (fx CT venografi til alle i denne population), så kan du ikke have gjort meget anderledes.
Vi forveksler ofte et dårligt outcome med dårlig diagnostik. Det er IKKE tilfældet, som Simon Carley fint illustrerer (St emlyns: making good decisions).
Sammenlign disse to forløb som er modificerede fra Simon Carleys blog:
- 32 årig mand kommer til akutmodtagelsen med sudden onset headache og blev bevistløs sekunder efter debut af hovedpinen. Nu har han det bedre, og han udskrives derfor. Kommer aldrig tilbage, og lever et normalt liv uden problemer, og får ikke de bivirkninger ved en CT skanning og LP kan give. Dårlig beslutning, godt outcome (Swadron et al: Pitfalls in the Management of Headache in the Emergency Department + Edlow 2018: Managing Patients With Nontraumatic, Severe, Rapid-Onset Headache)
- En 60 årig mand, kommer med brystsmerter 4 timer efter debut – har en HEART score <4 og TnI samt EKG er uden tegn til iskæmi. Han sendes hjem, men indlægges 14 dage efter med hjertesvigt og tegn på iskæmisk skade. God beslutning, dårligt outcome
Så med alt det vi ved om sandsynlighed for fejl, og hvor VIGTIGT det er, at vi som læger kan træffe disse beslutninger uden en pistol (eller en klagesag) som evig trussel, for patientens bedste (da alt andet fører til defensiv medicin og overdiagnostik) – hvorfor er vi så stadig hér?
Hvorfor taler vi ikke om acceptabel miss rate? Hvorfor uddannes vi ikke i kommunikation bedre, for at lindre patientens lidelse (og undgå klagesager)? Hvorfor findes der ikke organisterede og systematiske støttelementer for læger og andet sundhedspersonale i større udstrækning end i dag? Hvorfor er kulturen, at “fejl” skal man ikke tale om? hvorfor er vi kun interesserede i outcome, og ikke den diagnostiske tanke bagved?
Hvorfor roser vi den lungeemboli (outcome) man “fangede” som et “great catch”, og konkluderer, at vi skal “skanne mange flere på den måde” – på trods af, at man udførte en CT skanning på en patient med en Wells score på 0, och valgte ikke at bestille en d-dimer. Er det monstro mere sandsynligt, at den var falsk positiv? (Justin Morgenstern har lavet udregningen for dette):
“I frequently hear stories of “great catches”. Of doctors who ordered a CTPA, despite the patient being low risk for PE and PERC negative. Low and behold, the CT is positive. The doctor widely brags about this great save. Residents are taught about the fallibility of the PERC rule, and ultimately more CTs are ordered.
You can probably see where this is going. Let’s do that math. After an appropriate patient is ruled out by the PERC score, she has approximately a 1.4% chance of PE. (Kline 2004) A CT pulmonary angiogram is a pretty good test, although I have previously discussed data demonstrating that radiologists often disagree about the final read (Miller 2015) The best data we have probably comes from the PIOPED II study, which found that a CTPA has a 83% sensitivity and 96% specificity when compared to traditional pulmonary angiography. (Stein 2006) CT technology has changed since the PIOPED study, and so the sensitivity is almost certainly better (but I had a very hard time finding a modern estimate). For the sake of our calculations, I will just assume a 95% sensitivity.
Thus, for every 1000 low risk PERC negative patients seen in the ED, there will be 14 PEs. CT will catch 13 of these 14 patients. For the remaining 986 patients, CT will be falsely positive in 39. Therefore, the CT will be positive in 52 total patients, but only 13 of these patients (25%) actually have a PE.
So when a colleague brags about finding a PE in a low risk, PERC negative patient, there is a 75% chance they are wrong. There is a 75% chance that the patient has been given unnecessary anticoagulantion. A 75% chance that, although the CT was a false positive, the patient will rush to the emergency department for any chest pain or shortness or breath for the rest of her life, getting many more tests (and potentially more false positives). In other words, there is a 75% chance we are hurting this patient.You can’t interpret the results of a test without knowing the pretest probability. ” Justin Morgenstern, First10EM – why pretest probability is absolutely essential
Simon Carley har med stor visdom sagt (St emlyns: Making good decisions, 2016), at vi skal skelne good/bad decisions fra good/bad outcomes.
I figuren herover, har vi alle været i alle rammerne. Forhåbentligt er vi i vensre øvre/nedre hjørne for det meste. Men hvordan ved vi, at vi ikke er i højre øvre hjørne (højre nedre hjørne skal vi nok høre om – og hvis ikke, så skal vores samvittighed nok indhente os: Second Victim syndrome)
Feedback behøves for at vi kan vokse. En sikker levering af feedback uden dømmelse! (ellers formår vi aldrig at blive bedre, og vi gør kun folk bange for at være de læger, som patienten og vi som kollegaer, behøver)
Spørg til næste morgenmøde IKKE om en “spændende case”. Spørg om en kedelig case, men illustrerer beslutningsvejen! (jf fx dagens case fra dansk pædiatrisk selskab)
Klap din kollega på skulderen – vær åben som overlæge omkring fejl, og dine yngre læger forstår, at det er OK at tale om det (safe container). Vi må være det eksempel, vi ønsker vores kollegaer skal være for os, indtil et system er kommet på benene.

Det sker for os alle på et tidspunkt. Ser vi bort fra, at de fleste klagesager i større grad er et produkt af det system og de forhold vi arbejder under, og at individet ofte er årsagen til, at der netop IKKE kommer klagesager i et sådant system (jf Braithwaite 2018 – de 90% af tiden det går godt), så er der tider, hvor vi får personlige klager uden sikre store systemårsager. Vi er trods alt mennesker – og der sker noget interessant, uanset om der var belæg for klagen eller ej. Det påvirker vores fremtidige praksis. I værste fald, får vi alvorligt second victim syndrome og stopper måske som læger. I bedste fald sker der ingenting, men ofte vil vores praksis være påvirket i retning imod mere defensiv medicin til skade for vores patienter (jf Simon Carley: medical error).
Så hvorfor er klager overhoved noget, der eksisterer? Bør det ikke bare altsammen løses på system niveau, som det til dels gøres i Sverige? Hvorfor skal individet involveres?
Oftest føles det som om det er unødigt. Men måske er der noget for os som læger, som vi også kan tage med
Når vi får klager er det som en “immovable object” (lægen), der møder en “unstopable force” (patienten):
Lægen føler sig som et victim selv (second victim), og den faglige stolthed er på spil – til tider principper (særligt hvis man ikke lavede nogen fejl)
Vs
Patienten føler at noget er blevet taget fra dem, og de unødigt lider. Uanset hvem, der har sat de forventninger hele vejen derop (at dette ikke var en mulighed hele tiden i et probabilistisk sytem), så føler patienten det – og det kan vi aldrig ændre på. Patienten ønsker sjældent at skade lægen personligt, men er oftest selv medmenneskelig, og ønsker 1) at forstå, og 2) at se til, at det ikke sker igen for andre (i dette ligger der et slags behov for “meningsfuldhed” i deres lidelse, der ofte jo er meningsløs)
Så hvordan løser vi det hér, når det er sket? (udover at ringe til Yngre Læger / din fagforening, og tale med dine kollegaer)
Det vi som læger ofte gør fejl ved, er vi er defensive (faglig stolthed) og validerer ikke patientens lidelse (uanset hvem der har ret). Desuden forklarer vi ikke, hvad vi vil gøre for, at risikoen reduceres for at det sker igen.
Dr Matt Poyner (EmCases Ep 99) har lavet en liste som vi skal overveje i samtalen med patienten (hvis vi nogensinde kommer dertil):
– PREPARE – study the chart, respond within a week if possible
– APOLOGISE – there is always something to apologize for, whether it be for their suffering, that expectations were not met, or especially if an error was made. Apologizing is not admitting responsibility, it is showing empathy and a willingness to find a resolution.
– INFORM – explain what you did and why you did it; tell them you care about doing a good job
– NEXT STEPS – give assurance that something will be done to improve: extra reading, reviewing the case within your group, M&M rounds
Det letteste er selvfølgelig at undgå klagesager fra start: Skal du læse flere bøger? Sjældent er det problemet. Spender i stedet din tid på kommunikation og arbejdsmiljø: klagesager kan ikke fuldt undgås, men kan betydeligt reducres, hvis du viser empati og øver dine kommnunikations evner (ikke bare fordi du får færre klagesager – men for patienten og for at blive en bedre læge) (Smith et al, 2016: Does emergency physician empathy reduce thoughts of litigation? A randomised trial) -> se kommunikationsdelen af denne bog for råd
hovedkilde: Em Cases Ep 99 + 49 og 51
Litteratur om overdiagnostik er meget spredt, men nogle gode ting at starte med er
- Brodersen et al, 2018: overdiagnosis – what it is and what it isn’t
- BMJ artikel- og podcast serien “too much medicine”
- EmCases BCE Ep 72: Overinvestigation
- Overdiagnosis konferencen
- St emlyns: Risky business part 1-7
Og tolerating uncertainty
- Arabella Simpkins, 2016: Tolerating uncertainty – the new medical revolution
- Wray et al, 2016: The Diagnosis, Prognosis, and Treatment of Medical Uncertainty
- Greenberg: Over-testing: Why More Is Not Better
- Keijzers et al, 2018: Don’t just do something, stand there! The value and art of deliberate clinical inertia
Kilder til hele bloggen del 1-3 (foruden det linket i teksten)
- First10Em
- https://first10em.com/why-pretest-probability-is-essential/
- https://first10em.com/paying-patients-to-forgo-head-ct/
- https://first10em.com/cognitive-errors/
- St emlyns / Simon Carley / RCEM
- https://www.stemlynsblog.org/making-good-decisions-in-the-ed-rcem15/
- Wresting with risk, SMACC
- https://www.stemlynsblog.org/smacc2019-the-power-of-peer-review/
- Can we teach clinical judgement (carley, youtube)
- https://www.stemlynsblog.org/lessons-from-a-south-african-ed-kat-evans-at-stemlynslive/
- https://www.stemlynsblog.org/pulmonary-embolism-ambulatory-care-and-the-goddess-of-the-hunt/
- EmCrit
- Is Emergency Medicine a failed paradigme? (vimeo)
- BroomeDocs
- https://broomedocs.com/2016/11/smaccdub-bayes-2016-diagnostic-odyssey/
- EmCases og EMU 365
- EmCases Ep 47, 49, 51, 62 + 129
- WTBS 7: is triage obsolete?
- WTBS 17: https://emergencymedicinecases.com/why-warning-patients-to-stay-away-from-the-ed-will-never-work/
- EMU 365: Headache nightmares
- Artikler
- Sundblom og Dryver: Beslutsfattande på akuten
- Gallagher et al, 1997: Clinical Utility of Likelihood Ratios
- Braithwaite 2018: Changing how we think about healthcare improvement https://www.bmj.com/content/361/bmj.k2014
- Edlow 2018: Managing Patients With Nontraumatic, Severe, Rapid-Onset Headache
- Swadron, 2009: Pitfalls in theManagement of Headache in the Emergency Department
- Keijzers et al, 2018: Don’t just do something, stand there! The value and art of deliberate clinical inertia
- Coster, 2017: Why Do People Choose Emergency and Urgent Care Services? A Rapid Review Utilizing a Systematic Literature Search and Narrative Synthesis

