RESUS Quick-Review: D-dimer og præ-test sandsynlighed ved aortadissektion
Et hurtigt overblik - ikke et systematisk review - af den vigtigste litteratur på et område og, forhåbentlig, en konklusion på den kliniske anvendelighed

Case:
74-årig kvinde kendt med hypertension og osteoporose indbringes til akutmodtagelsen henvist fra egen læge obs AKS. Smerteforpint VAS 6 i ambulancen, BT 208/75, men ellers ABC-stabil og vågen, klar og orienteret. Givet 2 pust nitro med effekt. Ved ankomst til akutmodtagelsen ikke længere smertepåvirket.
Primær gennemgang:
A: Taler frit
B: SAT 96% u. ilttilskud, RF 17, egale og ubesværede thoraxbevægelser, stetoskopi med vesikulær respiration bilateralt uden bilyde
C: BT 156/63, P 93, kapillærrespons 2 sekunder, pæne farver, gode radialispulse bilateralt samt i femoralis på hø. side, men svær at palpere i ve. femoralis.
D: Vågen, klar og orienteret, ingen lateralisering eller oplagt facialisparese, BS 7,4
E: Temperatur 37,2 og ingen eksterne skader
Ved nærmere anamneseoptag har patienten igennem en uges tid haft intermitterende brystsmerter samt smerter i øvre del af ryggen, i starten omkring øvre del af ve. scapula, men nu rykket sig til lige under ve. scapula. Aktuelt smertefri. Smerterne beskrives som tiltagende, murrende, ikke pludseligt opståede og ikke oplagt forbundet med aktivitet. Pt. har ikke tidligere haft lignende smerter.
Paraklinik:
- Normale infektions-, væske- og lever/galdetal.
- 1. holds TnI 43 og D-Dimer 0,33
- EKG med sinusrytme frekvens 87, kendt venstresidigt grenblok, men ingen tegn til belastning eller akut iskæmi (vurderet med de modificerede Sgarbossa-kriterier)
- Røntgen thorax upåfaldende med normalt udseende mediastinum
Har patienten dissektion?
Dissektion er en af de "store 3" - differentialdiagnoserne vi ikke må overse hos patienter med brystsmerter: AKS, LE og aortadissektion. Alligevel er det en differentialdiagnose som det kan være svært at vide hvornår man skal undersøge nærmere for. Tilstanden er sjælden, med en forekomst beskrevet til 2-3/100.000/år i DK (1), men uden behandling er tilstanden dødelig med en mortalitet beskrevet til 25% efter 6 timer og 50% efter 24 timer (2). Alligevel er diagnosen i høj grad underdiagnosticeret i akutafdelingen med en miss-rate på op til 33,8%(3) og vi tænker formentligt for sjældent på den. Smider vi alle patienter med brystsmerter i CT-scanneren gør vi dog med sikkerhed skade.
Det traditionelle "kardinalsymptom" i DK, brystsmerter udstrålende til ryggen, er ikke sensitivt, med en sensitivitet beskrevet helt ned til 32% i en meta-analyse fra 2002 over symptomer på thorakale dissektioner (3) og det er vigtigt at bevare opmærksomheden på diagnosen også ved fraværet af dette symptom. Andre symptomer der også er beskrevet i meta-analysen er angivet i tabellen nedenfor med deres respektive Likelihood Ratios (ikke-signifikante resultater markeret med grå)
| Symptom | Positiv likelihood ratio | Negativ likelihood ratio |
| Skærende/rivende smertekvalitet | 10,8 [5,2-22] | 0,4 [0,3-0,5] |
| Migrerende/flyttende smerte | 7,6 [3,6-16] | 0,6 [0,5-0,7] |
| Pludseligt indsættende smerte | 2,6 [2,0-3,5] | 0,3 [0,2-0,4] |
| Kendt hypertension | 1,5 [0,8-3,0] | 0,4 [0,3-0,6] |
| Pulsdeficit | 2,7 [0,7-9,8] | 0,63 [0,4-1,0)] |
| Fokalt neurologisk udfald | 33 [2,0-549] | 0,87 [0,8-0,9] |
De inkluderede studier er dog præget af primært at være retrospektive og er generelt ikke af høj kvalitet med inkluderede studier helt tilbage fra 1950. Et nyere studie fra 2017, udført i akutafdelingen (4), finder noget bedre performance for de enkelte tegn, med f.eks. en LR- for pludseligt indsættende smerte på 0,07, men med generelt set enorme konfidensintervaller, formentligt på baggrund af dets lille population og dermed sample size bias (194 cases og 776 kontroller) samt retrospektive case-kontrol form, som næsten garanterer et verification bias.
Konklusionen må nok være at det på den foreliggende evidens er meget svært sikkert at udelukke aortadissektion ud fra anamnese og klinisk undersøgelse.
Vores patient i casen ovenover har ikke umiddelbart beskrevet pludseligt indsættende eller skærende/rivende smertekvalitet, men har migrerende smerter og en mulig pulsdeficit samt kendt hypertension. I bedste tilfælde havner vi måske tilbage på den oprindelige præ-test sandsynlighed efter anamneseoptag og kan i hvert fald ikke udelukke diagnosen på dette når vi nu har fået mistanken om at denne patient kunne have en aortadissektion. Hvordan skal vi så komme det nærmere?
D-dimer og dissektion
Hov, vent! Patienten har en "negativ" d-dimer på 0,33. Så er aortadissektion vel udelukket?
Anvendeligheden af d-dimer til at bestyrke eller afkræfte mistanken om en aortadissektion har været omdiskuteret. En nylig meta-analyse fra Journal of Cardiothoracic Surgery fra 2021 finder da også en ganske imponerende sensitivitet på 0,96 [0,91-0,98] med en specificitet på 0,7 [0,57-0,81], dog med en betydelig heterogenicitet i studierne (5). Det giver os dog følgende likelihood ratios:
- Positiv likelihood ratio (ved positiv d-dimer): 3,25 [2,18-4,85]
- Negativ likelihood ratio (ved negativ d-dimer): 0,06 [0,03-0,12]
Går vi videre med vores tankeeksperiment ud fra patientcasen ovenfor kan vi opstille følgende to scenarier:
Scenarie 1:
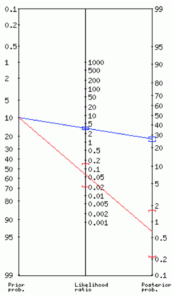
- Går vi ud fra en mavefornemmelse om at patienten havde en præ-test sandsynlighed på 10% (trods alt ikke tale om pludseligt indsættende, skærende smerter, men intermitterende over en uge og differentialdiagnose AKS trods alt stadig inde i billedet) falder post-test sandsynligheden ved negativ D-dimer til 0,7%
Scenarie 2:
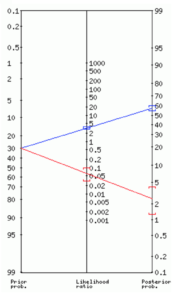
- Skyder vi derimod præ-test sandsynligheden til 30% (kendt hypertension og migrerende smerter lokaliseret til ryggen samt puls-deficit foruden nu mindre sandsynlighed for AKS efter normalt EKG og TnI) falder den kun til 3% efter negativ D-dimer
Acceptable miss rate og overdiagnosticering
En post-test sandsynlighed på 1-3% kan synes overordentlig lille og umiddelbart som ensbetydende med en udelukket diagnose. Ser vi dog på tallene fra en anden vinkel vil de betyde at vi overser en aortadissektion hos ca 1 ud af 50 patienter med disse symptomer. For så alvorlig en diagnose som aortadissektion skal vi måske tænke os om en ekstra gang før vi accepterer en så høj miss-rate. Havde der været tale om en mere benign tilstand såsom dyspepsi eller viral øvre luftvejsinfektion havde en overset diagnose hos 1-3% bestemt været acceptabel.
Risikoen ved overset diagnose skal sættes op imod den indbårne risiko ved yderligere udredning - såsom akut nyresvigt, bestråling eller fund af "incidentalomer" ved CT-scanning og den medfølgende "cascade of care" i form af f.eks. invasive diagnostiske indgreb og deres potentielle komplikationer.
Studier der tidligere har undersøgt hvor den diagnostiske tærskel for CT angio - sandsynligheden hvor den potentielle gavn ved yderligere udredning med CT angio udvejer risikoen - bør ligge sætter den imellem 0,3%-2%(6) og vi befinder os således kun et sted lige i den øvre del af denne tærskel hos vores aktuelle patient, selv efter en negativ d-dimer.
Vender vi kikkerten og ser på konsekvenserne ved anvendelse af d-dimer i diagnosticeringen af aortadissektion på populationsbasis kommer den noget lavere specificitet pludseligt til at få en særlig betydning. Tager vi en d-dimer på 1000 patienter med brystsmerter med en præ-test sandsynlighed på 30% vil 300 af dem have dissektion, mens 700 ikke vil. Til gengæld vil 210 af de der ikke har dissektion have en positiv d-dimer og dermed kræve en CT-scanning.
| 30% præ-test | Har dissektion | Har ikke dissektion | Total |
| Positiv d-dimer | 288 | 210 | 498 |
| Negativ d-dimer | 12 | 490 | 502 |
| Total | 300 | 700 | 1000 |
Kigger vi på det andet (og måske mere sandsynlige eksempel) med en præ-test sandsynlighed på 10% falder raten af sandt positive vs. falsk positive og vi scanner faktisk flere patienter unødvendigt.
| 10% præ-test | Har dissektion | Har ikke dissektion | Total |
| Positiv d-dimer | 96 | 270 | 366 |
| Negativ d-dimer | 4 | 630 | 634 |
| Total | 100 | 900 | 1000 |
Den sande præ-test sandsynlighed for en bred population af patienter med brystsmerter er formentligt væsentligt lavere, måske helt ned til 2%, hvilket vil resultere i at vi for at finde 19 dissektioner og "kun" overse 1 i en population på 1000 skal scanne 294 patienter unødvendigt.
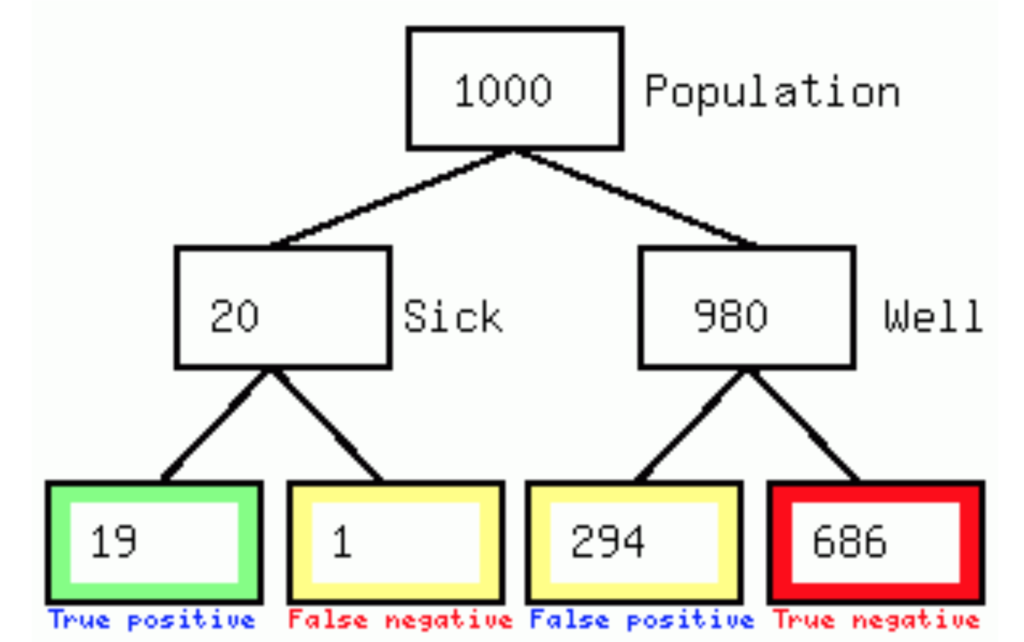
Den forholdsvist lave prævalens af diagnosen gør altså en test som d-dimer med en relativt lav specificitet, trods en ganske god sensitivitet, svær at anvende på en større population, da den med høj sandsynlighed vil føre til en betydelig overdiagnosticering og dermed videre udredning og potentiale for unødvendig patientskade.
Den kliniske bundlinje
Selv ved anvendelsen på den enkelte patient i vores tilfælde med et relativt broget anamnestisk og klinisk billede og dermed relativt lav præ-test sandsynlighed giver d-dimer os kun en post-test sandsynlighed der i bedste fald lander i den øvre del af den diagnostiske tærskel. Vi må derfor formentligt gå videre med en CT-scanning under alle omstændigheder, når vi nu først er gået igang med at undersøge for puls-deficit og lignende og dermed altså har haft en præ-test sandsynlighed høj nok til at gå igang med udredning.
På befolkningsniveau - og måske særligt i den brogede patientpopulation vi ser i akutafdelingen - synes d-dimer blot at føre til en uacceptabel overdiagnosticering. Konklusionen må altså synes at være at d-dimer ikke er anvendelig i udredningen af aortadissektion og såfremt vi først har fået en mistanke der er stærk nok til at overveje at tage en d-dimer bør vi formentligt blot gå direkte videre med en CT-angiografi for sikkert at be- eller afkræfte diagnosen.
Det betyder dog ikke at d-dimer ikke på et tidspunkt kan komme i spil på andre måder og den er f.eks. blevet undersøgt i kombination med en allerede valideret (men for nuværende ikke særligt anvendelig) risikoscore kaldet Aortic Dissection Detection Risk Score (ADD-RS) som scorer patienter fra 0-3 point baseret på risikofaktorer, risikosymptomer og risikofund(7):
- Risikofaktorer:
- Marfan, familiær disposition, kendt aortaklapsygdom, nylig aortamanipulation eller kendt thorakalt aortaaneurisme
- Risikosymptomer:
- Bryst-, ryg- eller mavesmerter beskrevet som pludseligt indsættende, svær intensitet eller skærende
- Risikofund:
- Pulsdeficit, forskel i systolisk BT på modsidige ekstremiteter, fokale neurologiske udfald, ny systolisk mislyd (med smerte) eller hypotension/shock
For nuværende er ADD-RS bundet op på en noget uklar algoritme hvor en score på 0-1 medfører med røntgen thorax og udredning for andre årsager, mens en score på ≥2 udløser en CT angiografi. Et prospektivt observationelt multicenterstudie fra 2018 undersøgte kombinationen af ADD-RS med d-dimer og fandt i en population på 1850 patienter, hvoraf 241 havde dissektion, en rate for oversete cases på 0,3% (og altså helt nede i den lave ende af den diagnostiske tærskel) ved kombinationen af ADD-RS med d-dimer. Studiet mangler dog ekstern validering og dets observationelle natur lægger op til en række potentielle bias, hvorfor denne strategi desværre formentligt ikke ligger lige umiddelbart foran os.
Udsigten til potentielt at få en klinisk anvendelig pathway til sikker udelukkelse af aortadissektion lig Wells+PERC scorerne for lungeemboli er dog lovende for denne patientgruppe som i høj grad for nuværende overses, da det potentielt vil kunne føre til en større bekvemmelighed ved hyppigere at overveje diagnosen i akutafdelingen, hvor vi for nuværende desværre synes at overse den ellers sjældne diagnose i en uacceptabel grad.
Har du fået mere blod på tanden ift. at læse op på evidensen bag dissektion og d-dimer har Justin Morgenstern fra First10EM som altid lavet en gennemgang som på alle måder sætter denne til skamme.
Referencer
- Lægehåndbogen: Aortadissektion. Fagligt opdateret: https://www.sundhed.dk/sundhedsfaglig/laegehaandbogen/hjerte-kar/tilstande-og-sygdomme/karsygdomme/aortadissektion/
- Kenneth J. Cherry, Michael D. Dake, chapter 31 - Aortic Dissection, Comprehensive Vascular and Endovascular Surgery (Second Edition), Mosby, 2009, Pages 517-531, ISBN 9780323057264, https://doi.org/10.1016/B978-0-323-05726-4.00033-0.
- Lovatt S, Wong CW, Schwarz K, Borovac JA, Lo T, Gunning M, Phan T, Patwala A, Barker D, Mallen CD, Kwok CS. Misdiagnosis of aortic dissection: A systematic review of the literature. Am J Emerg Med. 2022 Mar;53:16-22. doi: 10.1016/j.ajem.2021.11.047. Epub 2021 Dec 4. PMID: 34968970.
- Klompas M. Does this patient have an acute thoracic aortic dissection? JAMA. 2002 May 1;287(17):2262-72. doi: 10.1001/jama.287.17.2262. PMID: 11980527.
-
Ohle R, Um J, Anjum O, Bleeker H, Luo L, Wells G, Perry JJ. High Risk Clinical Features for Acute Aortic Dissection: A Case-Control Study. Acad Emerg Med. 2018 Apr;25(4):378-387. doi: 10.1111/acem.13356. Epub 2018 Jan 15. PMID: 29218798.
-
Yao J, Bai T, Yang B, Sun L. The diagnostic value of D-dimer in acute aortic dissection: a meta-analysis. J Cardiothorac Surg. 2021 Nov 27;16(1):343. doi: 10.1186/s13019-021-01726-1. PMID: 34838062; PMCID: PMC8627055.
-
Taylor RA, Iyer NS. A decision analysis to determine a testing threshold for computed tomographic angiography and D-dimer in the evaluation of aortic dissection. Am J Emerg Med. 2013 Jul;31(7):1047-55. doi: 10.1016/j.ajem.2013.03.039. Epub 2013 May 20. PMID: 23702073.
-
Rogers AM, Hermann LK, Booher AM, Nienaber CA, Williams DM, Kazerooni EA, Froehlich JB, O'Gara PT, Montgomery DG, Cooper JV, Harris KM, Hutchison S, Evangelista A, Isselbacher EM, Eagle KA; IRAD Investigators. Sensitivity of the aortic dissection detection risk score, a novel guideline-based tool for identification of acute aortic dissection at initial presentation: results from the international registry of acute aortic dissection. Circulation. 2011 May 24;123(20):2213-8. doi: 10.1161/CIRCULATIONAHA.110.988568. Epub 2011 May 9. PMID: 21555704.
-
Nazerian P, Mueller C, Soeiro AM, Leidel BA, Salvadeo SAT, Giachino F, Vanni S, Grimm K, Oliveira MT Jr, Pivetta E, Lupia E, Grifoni S, Morello F; ADvISED Investigators. Diagnostic Accuracy of the Aortic Dissection Detection Risk Score Plus D-Dimer for Acute Aortic Syndromes: The ADvISED Prospective Multicenter Study. Circulation. 2018 Jan 16;137(3):250-258. doi: 10.1161/CIRCULATIONAHA.117.029457. Epub 2017 Oct 13. PMID: 29030346.
- Morgenstern, J. D-dimer for aortic dissection: the evidence, First10EM, February 7, 2017. Available at:
https://doi.org/10.51684/FIRS.3932